题目内容
电量计是由电解质溶液和置于其中的两个电极所构成.使用时,将其串联到电路中,通电一段时间后,精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,用法拉第定律求出所通过的电量.已知电极上每通过96500C的电量就会有1mol电子发生转移. 实际测量中,常用银电量计,如图所示.下列说法正确的是( )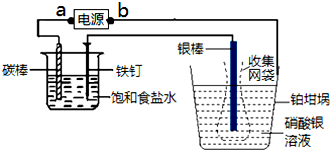

| A、a为电源的负极,铂坩埚为阳极 |
| B、称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0 mg,则电解过程中通过电解池的电量为96500C |
| C、实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋.若没有收集网袋,测量结果会偏高 |
| D、铁钉和碳棒上都有气泡产生,若加入酚酞试剂,先在碳棒附近溶液变红色 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、根据银电量计的电解原理判断电极反应,从而确定电源的正负极;
B、测得铂坩埚增重,就能知道阳极有多少银被腐蚀,从而算出通过的电量;
C、电解时阳极的银容易脱落而影响实验结果;
D、电解食盐水时,阴极附近显碱性.
B、测得铂坩埚增重,就能知道阳极有多少银被腐蚀,从而算出通过的电量;
C、电解时阳极的银容易脱落而影响实验结果;
D、电解食盐水时,阴极附近显碱性.
解答:
解:A、电解时的电极反应为:阳极(Ag):Ag-e-═Ag+,阴极(Pt):Ag++e-═Ag,所以a为正极,铂坩埚为阴极,故A错误;
B、析出Ag的物质的量为
=1mmol=0.001mol,根据Ag++e-=Ag可知通过的电子物质的量为0.001mol,通过电量为96.5C,故B错误;
C、银溶解时有些可能未失电子变成银离子然后在阴极(铂坩埚)得电子析出,而是直接跌落到铂坩埚中,造成铂坩埚增重较多,导致计算出的电量偏大,所以必须增加收集袋,故C正确;
D、电解食盐水时,阴极附近显碱性,所以铁钉附近溶液变红,故D错误;
故选C.
B、析出Ag的物质的量为
| 108.0mg |
| 108.0g/mo |
C、银溶解时有些可能未失电子变成银离子然后在阴极(铂坩埚)得电子析出,而是直接跌落到铂坩埚中,造成铂坩埚增重较多,导致计算出的电量偏大,所以必须增加收集袋,故C正确;
D、电解食盐水时,阴极附近显碱性,所以铁钉附近溶液变红,故D错误;
故选C.
点评:本题考查电解原理的应用,注意电解池的组成和两极上的变化,并注意与电镀知识的结合来分析解答即可.

练习册系列答案
相关题目
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:根据上述实验,以下说法正确的是( )
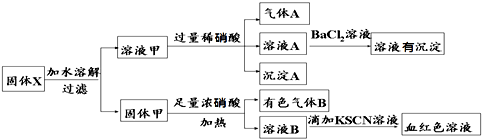

| A、气体A一定只是NO |
| B、由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C、若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D、溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |
下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是( )
| A、H2SO4 |
| B、KOH |
| C、BaCl2 |
| D、Na2CO3 |
常温下,向等物质的量浓度的两种一元酸的盐溶液中,分别通入少量的CO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3;2NaB+CO2+H2O=2HB+Na2CO3,则等物质的量浓度的HA和HB在水中电离出H+的能力大小关系是( )
| A、HA较强 | B、HB较强 |
| C、两者一样 | D、无法比较 |
下列哪项做法,不能有助于能源“开源节流”( )
| A、大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
| B、减少资源消耗,增加资源的重复利用、资源的循环再生 |
| C、发展低碳经济,推广利用电能、风能的城市照明系统 |
| D、大力开采煤、石油和天然气以满足人们日益增长的能源需求 |
下列说法不正确的是( )
| A、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
| B、用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| D、分子式为C4H10O并能与金属钠反应放出氢气的有机化合物有4种 |
100℃时将pH为8的NaOH溶液与pH为10的NaOH溶液等体积混合后,溶液中氢离子浓度为( )
A、
| ||
B、
| ||
C、
| ||
| D、(1×10-14-5×10-5) mol/L |
下列有关胶体的说法正确的是( )
| A、胶体一定是混合物 |
| B、胶体与溶液的本质区别是有丁达尔效应 |
| C、将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D、胶体属于介稳体系 |