题目内容
元素X和Y属于同一主族.负二价的元素X和氢的化合物在通常状况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%.
(1)在元素X和元素Y两种元素形成的化合物中,写出X质量分数为50%的化合物的化学式 ;该分子中中心原子以 杂化,分子构型 .
(2)写出X的质量分数为60%的化合物的化学式 ;该分子中中心原子以 杂化,分子构型 .
(3)由元素氢、X、Y三种元素形成的化合物常见的有两种,其水溶液呈酸性,试分别写出其分子式 、 ,并比较酸性强弱: .
(4)酸性较强的酸根离子的空间构型为 .
(1)在元素X和元素Y两种元素形成的化合物中,写出X质量分数为50%的化合物的化学式
(2)写出X的质量分数为60%的化合物的化学式
(3)由元素氢、X、Y三种元素形成的化合物常见的有两种,其水溶液呈酸性,试分别写出其分子式
(4)酸性较强的酸根离子的空间构型为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:负二价的元素X和氢的化合物在通常情况下是一种液体,其中X的质量分数为88.9%,负二价的元素X和氢的化合物为H2X,令X的相对分子质量为a,则
=88.9%,解得a=16,所以X为氧元素;元素X和Y属于同一主族,处于ⅥA族,元素X和元素Y可以形成两种化合物为YO2和YO3,YO2和YO3中O的质量分数分别为50%和60%,令Y的相对原子质量为b,则
=1-50%,解得b=32,则Y为硫元素,所以两种化合物为SO2和SO3,据此答题;
| a |
| a+2 |
| b |
| b+32 |
解答:
解:负二价的元素X和氢的化合物在通常情况下是一种液体,其中X的质量分数为88.9%,负二价的元素X和氢的化合物为H2X,令X的相对分子质量为a,则
=88.9%,解得a=16,所以X为氧元素;元素X和Y属于同一主族,处于ⅥA族,元素X和元素Y可以形成两种化合物为YO2和YO3,YO2和YO3中O的质量分数分别为50%和60%,令Y的相对原子质量为b,则
=1-50%,解得b=32,则Y为硫元素,所以两种化合物为SO2和SO3,
(1)根据上面的分析可知,X质量分数为50%的化合物的化学式为SO2,分子中中心原子硫原子的价层电子对数为
=3,所以硫原子以sp2方式杂化,由于分子中有一对孤电子对,所以分子的空间构型为V形,
故答案为:SO2;sp2;V形;
(2)根据上面的分析可知,X质量分数为60%的化合物的化学式为SO3,分子中中心原子硫原子的价层电子对数为
=3,所以硫原子以sp2方式杂化,由于分子硫原子没有孤电子对,所以分子的空间构型为平面三角形,
故答案为:SO3;sp2;平面三角形;
(3)由元素氢、X、Y三种元素形成的他合物常见的有两种,其水溶液均显酸性,则两种物质为H2SO4、H2SO3,酸性强弱为H2SO4>H2SO3.
故答案为:H2SO4;H2SO3;H2SO4>H2SO3;
(4)酸性较强的酸根离子为硫酸根离子,在硫酸根离子中,硫原子的价层电子对数为
=4,硫原子没有孤电子对,所以它的空间构型为正四面体,
故答案为:正四面体;
| a |
| a+2 |
| b |
| b+32 |
(1)根据上面的分析可知,X质量分数为50%的化合物的化学式为SO2,分子中中心原子硫原子的价层电子对数为
| 6+0 |
| 2 |
故答案为:SO2;sp2;V形;
(2)根据上面的分析可知,X质量分数为60%的化合物的化学式为SO3,分子中中心原子硫原子的价层电子对数为
| 6+0 |
| 2 |
故答案为:SO3;sp2;平面三角形;
(3)由元素氢、X、Y三种元素形成的他合物常见的有两种,其水溶液均显酸性,则两种物质为H2SO4、H2SO3,酸性强弱为H2SO4>H2SO3.
故答案为:H2SO4;H2SO3;H2SO4>H2SO3;
(4)酸性较强的酸根离子为硫酸根离子,在硫酸根离子中,硫原子的价层电子对数为
| 6+2 |
| 2 |
故答案为:正四面体;
点评:本题主要考查了原子杂化轨道、分子空间构型等知识点,难度不大,解题的关键在于根据物质组成确定元素种类.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
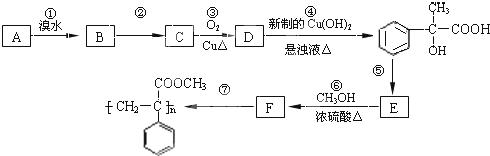
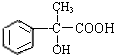 的分子式
的分子式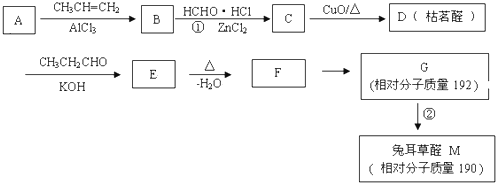
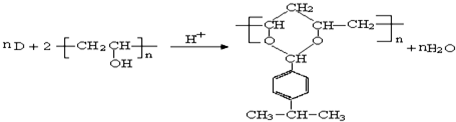
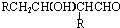
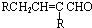
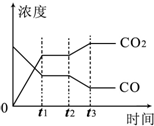 对于反应CO(g)+H2O(g)?H2(g)+CO2(g)
对于反应CO(g)+H2O(g)?H2(g)+CO2(g)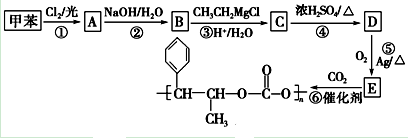
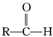 +R′-M′gX→
+R′-M′gX→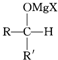
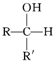 (R,R′均为烃基)
(R,R′均为烃基)