题目内容
 BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如下两种.下列说法不正确的是( )
出发合成BHT的方法有如下两种.下列说法不正确的是( )| A、推测BHT在水中的溶解度小于苯酚 |
B、BHT与 都能使酸性KMnO4退色 都能使酸性KMnO4退色 |
| C、方法一和方法二的反应类型都是加成反应 |
D、BHT与 具有完全相同的官能团 具有完全相同的官能团 |
考点:有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:A.烃基为憎水基,BHT中烃基数目比苯酚多,溶解性一定小于苯酚;
B.酚羟基都能够被强氧化剂氧化;
C.反应一为加成,反应二为取代;
D.BHT中含有的官能团是酚羟基.
B.酚羟基都能够被强氧化剂氧化;
C.反应一为加成,反应二为取代;
D.BHT中含有的官能团是酚羟基.
解答:
解:A.BHT中含有的憎水基烃基比苯酚多,所以在水中的溶解度小于苯酚,故A正确;
B.BHT和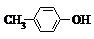 中都会有酚羟基,都能够被酸性高锰酸钾溶液氧化二使酸性KMnO4褪色,故B正确;
中都会有酚羟基,都能够被酸性高锰酸钾溶液氧化二使酸性KMnO4褪色,故B正确;
C、反应一通过加成反应生成BHT,而反应二为取代反应,故C错误;
D、BHT中含有的官能团是酚羟基, 中含有的官能团也是酚羟基,故D正确,
中含有的官能团也是酚羟基,故D正确,
故选C.
B.BHT和
 中都会有酚羟基,都能够被酸性高锰酸钾溶液氧化二使酸性KMnO4褪色,故B正确;
中都会有酚羟基,都能够被酸性高锰酸钾溶液氧化二使酸性KMnO4褪色,故B正确;C、反应一通过加成反应生成BHT,而反应二为取代反应,故C错误;
D、BHT中含有的官能团是酚羟基,
 中含有的官能团也是酚羟基,故D正确,
中含有的官能团也是酚羟基,故D正确,故选C.
点评:本题考查了有机物结构与性质、绿色化学的判断,题目难度中等,注意掌握常见的有机物的结构与性质,明确绿色化学的概念及要求,熟悉常见的有机反应类型.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在恒容的密闭容器中,可逆反应X(s)+3Y(g)?2Z(g)△H>0,达到平衡时,下列说法正确的是( )
| A、充入少量He使容器内压强增大,平衡向正反应方向移动 |
| B、升高温度,平衡向正反应方向移动,容器内压强一定减小 |
| C、继续加入少量X,X的转化率减小,Y的转化率增大 |
| D、继续加入少量Y,再次平衡时,Y的体积分数一定比上次平衡小 |
下列溶液中各微粒的浓度关系正确的是( )
| A、0.1 mol?L-1 NaHSO4溶液中:[Na+]>[SO42-]>[H+]>[OH-] |
| B、0.1 mol?L-1Na2S溶液中:2[Na+]=[S2-]+[HS-]+[H2S] |
| C、0.1 mol?L-1 NaHCO3溶液中:[Na+]+[H+]=[HCO3-]+2[CO32-]+[OH-] |
| D、等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:[Na+]=[CH3COO-]>[H+]=[OH-] |
某未知溶液中已检验出含有离子Ca2+、NO3-,且pH=2.欲检验此溶液中是否大量存在以下6种离子:①ClO- ②NH4+③I-④Fe2+⑤AlO2-⑥Cl-,其中不必检验就能排除的离子是( )
| A、②③⑤⑥ | B、①③④⑤ |
| C、①④⑤⑥ | D、①②③④ |
下列物质属于高分子化合物的是( )
| A、油脂 | B、淀粉 |
| C、高级脂肪酸 | D、氨基酸 |
2005年6月5日 是第34个世界环境日,联合国环境署确定2005年活动主题是“营造绿色城市,呵护地球家园”.我国环境总局确定的主题是“人人参与创建绿色家园”.下列做法不符合这一主题的是( )
| A、回收废旧电池 |
| B、加强燃放烟花爆竹法规 |
| C、停止使用含铅汽油 |
| D、将工厂烟囱加高,减少周围大气污染 |
由于催化作用使反应速率加快的是( )
| A、乙酸乙酯水解,加入氢氧化钠溶液 |
| B、苯与液溴反应,加入少量铁粉 |
| C、实验室制取甲烷时,加入生石灰 |
| D、锌与盐酸反应,加入少量浓硫酸 |
 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3
如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3| 放电 |
| 充电 |
| A、放电过程中钠离子从左到右通过离子交换膜 |
| B、电池放电时,负极反应为:3NaBr-2e-=NaBr3+2Na+ |
| C、充电过程中钠离子在右边电极区域放电 |
| D、充电的过程中当0.1molNa+通过离子交换膜时,导线通过0.1mol电子 |
由原子轨道相互重叠形成的σ键和π键总称价键轨道,是分子结构的价键理论中最基本的组成部分.关于该理论下列有关认识不正确的是( )
| A、σ键不属于共价键 |
| B、s-sσ键与s-pσ键都是轴对称 |
| C、分子中含有共价键,则至少含有一个σ键 |
| D、含有π键的化合物与只含σ键的化合物的化学性质不同 |