题目内容
已知浓硫酸和木炭粉在加热条件下可发生化学反应.
(1)浓硫酸与木炭粉加热反应的化学方程式为: .
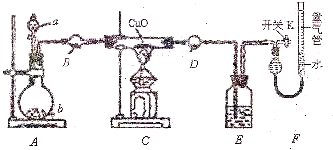
(2)试用如图中所列各装置设计一个实验,验证上述反应所产生的各种产物.这种装置的连接顺序(按产物气流从左到右的方向)是(填图中装置的编号): → → → .
(3)实验时可观察到装置①中,A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是: ,B瓶溶液的作用是 ,C瓶溶液的作用是 .
(4)装置②中所加的白色固体药品是 ,可验证的产物是 .
(5)装置③中所盛的溶液是 ,可验证的产物是 .
(6)在各装置所盛的试剂不变的条件下,若装置的连接顺序为④→①→②→③,则可以检出的产物是 (填化学式,下同),不能检出的产物是 .
| 编号 | ① | ② | ③ | ④ |
| 装置 |  | 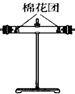 | 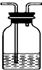 | 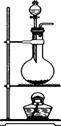 |
(2)试用如图中所列各装置设计一个实验,验证上述反应所产生的各种产物.这种装置的连接顺序(按产物气流从左到右的方向)是(填图中装置的编号):
(3)实验时可观察到装置①中,A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是:
(4)装置②中所加的白色固体药品是
(5)装置③中所盛的溶液是
(6)在各装置所盛的试剂不变的条件下,若装置的连接顺序为④→①→②→③,则可以检出的产物是
考点:性质实验方案的设计,浓硫酸的性质实验
专题:
分析:(1)木炭粉与浓硫酸发生反应产生SO2和CO2气体;
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳;
(3)根据实验目的和装置图考虑操作步骤和试剂的作用及发生反应.从整体考虑,A为检验二氧化硫装置,B、C为除去二氧化硫并检验是否除尽二氧化硫的装置;
(4)无水硫酸铜为白色固体,遇水可变为五水硫酸铜(CuSO4?5H2O)为蓝色固体;
(5)根据CO2能使澄清石灰水变浑浊;
(6)因为先通入①,溶液中会有水蒸汽出来,则无法说明开始反应是否有水蒸汽产生,所以若装置的连接顺序为④→①→②→③,可以检验的产物为SO2和CO2气体,不能检出的产物是H2O.
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳;
(3)根据实验目的和装置图考虑操作步骤和试剂的作用及发生反应.从整体考虑,A为检验二氧化硫装置,B、C为除去二氧化硫并检验是否除尽二氧化硫的装置;
(4)无水硫酸铜为白色固体,遇水可变为五水硫酸铜(CuSO4?5H2O)为蓝色固体;
(5)根据CO2能使澄清石灰水变浑浊;
(6)因为先通入①,溶液中会有水蒸汽出来,则无法说明开始反应是否有水蒸汽产生,所以若装置的连接顺序为④→①→②→③,可以检验的产物为SO2和CO2气体,不能检出的产物是H2O.
解答:
解:(1).木炭粉与浓硫酸发生反应产生SO2和CO2气体,反应的方程式为2H2SO4(浓)+C
2SO2↑+CO2↑+2H2O,
故答案为:2H2SO4(浓)+C
2SO2↑+CO2↑+2H2O;
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳,故答案为:④;②;①;③;
(3)A为检验二氧化硫装置,B、C为除去二氧化硫并检验是否除尽二氧化硫的装置,故答案为:检验SO2气体;吸收SO2气体;检验SO2气体是否除干净;
(4)无水硫酸铜为白色固体,遇水可变为五水硫酸铜(CuSO4?5H2O)为蓝色固体,用于检验水的存在,故答案为:无水硫酸铜;H2O;
(5)将气体通入澄清石灰水中,石灰水变浑浊,所以证明该气体是CO2,故答案为:澄清石灰水;CO2;
(6)因为先通入①,溶液中会有水蒸汽出来,则无法说明开始反应是否有水蒸汽产生,所以若装置的连接顺序为④→①→②→③,可以检验的产物为SO2和CO2气体,不能检出的产物是H2O,故答案为:SO2和CO2;H2O;
| ||
故答案为:2H2SO4(浓)+C
| ||
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳,故答案为:④;②;①;③;
(3)A为检验二氧化硫装置,B、C为除去二氧化硫并检验是否除尽二氧化硫的装置,故答案为:检验SO2气体;吸收SO2气体;检验SO2气体是否除干净;
(4)无水硫酸铜为白色固体,遇水可变为五水硫酸铜(CuSO4?5H2O)为蓝色固体,用于检验水的存在,故答案为:无水硫酸铜;H2O;
(5)将气体通入澄清石灰水中,石灰水变浑浊,所以证明该气体是CO2,故答案为:澄清石灰水;CO2;
(6)因为先通入①,溶液中会有水蒸汽出来,则无法说明开始反应是否有水蒸汽产生,所以若装置的连接顺序为④→①→②→③,可以检验的产物为SO2和CO2气体,不能检出的产物是H2O,故答案为:SO2和CO2;H2O;
点评:本题考查学生浓硫酸的性质中的和碳单质的反应,注意产物检验所用的试剂以及检验的先后顺序知识,综合性较强,难度大.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
除去混在碳酸钠粉末中的少量碳酸氢钠,最合理的方法是( )
| A、加盐酸 | B、加水 |
| C、加热 | D、加NaOH溶液 |
下列有关工业生产的叙述正确的是( )
| A、合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率 |
| B、从海水中提镁过程中,电解熔融MgO可制备Mg |
| C、电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小 |
| D、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
以下对生活事实的解释,不正确的是( )
| A、食品添加剂虽然能改善食物的色、香、味,但由于他们对健康有害,均不宜食用 |
| B、厨房里洗涤油污,常用碱性洗涤剂,因为植物油会在碱性溶液中水解 |
| C、用灼烧的方法可以区别人造丝和蚕丝,因为蚕丝是蛋白质,灼热时产生具有烧焦羽毛的气味 |
| D、高温消毒是通过加热的方法使细菌的蛋白质变性而死亡 |
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下: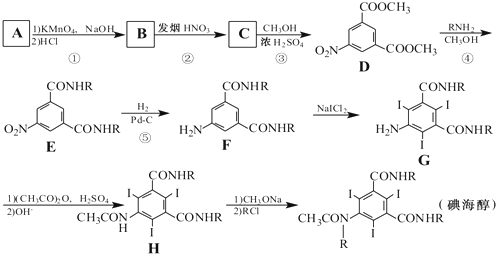
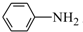 呈弱碱性,易被氧化请写出以和(CH3CO)2O为原料制备染料中间体
呈弱碱性,易被氧化请写出以和(CH3CO)2O为原料制备染料中间体 的合成路线流程图(无机试剂任用)
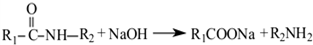
的合成路线流程图(无机试剂任用) +CH3COOH
+CH3COOH +H2O
+H2O 注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: