题目内容
化学无处不在,下列与化学有关的说法不正确的是( )
| A、电镀的酸性废液用碱中和后还是不可以排放 |
| B、侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| C、碘是人体必需微量元素,所以要多吃富含KIO3的食盐 |
| D、室温下,AgCl在水中的溶解度小于在食盐中的溶解度 |
考点:"三废"处理与环境保护,纯碱工业(侯氏制碱法),难溶电解质的溶解平衡及沉淀转化的本质,微量元素对人体健康的重要作用
专题:基本概念与基本理论,化学应用
分析:A.酸性废液用碱中和后,溶液呈中性可以排放;
B.二氧化碳在水中溶解度较小,但是在碱性环境条件下溶解性很大;
C.碘是人体必须微量元素,每人每天大约吃食盐12克,多吃无益;
D.在AgCl溶液中存在AgCl(s)?Ag+(aq)+Cl-(aq),从沉淀平衡移动的角度分析.
B.二氧化碳在水中溶解度较小,但是在碱性环境条件下溶解性很大;
C.碘是人体必须微量元素,每人每天大约吃食盐12克,多吃无益;
D.在AgCl溶液中存在AgCl(s)?Ag+(aq)+Cl-(aq),从沉淀平衡移动的角度分析.
解答:
解:A.电镀的酸性废液滴加碱至恰好完全应,溶液呈中性时,符合绿色排放标准,可以排放,故A错误;
B.二氧化碳在水中溶解度较小,但是在碱性环境条件下溶解性很大,所以在侯氏制碱法中应该先通入氨气然后再通入二氧化碳,故B正确;
C.碘是人体必需微量元素,所以要吃富含KIO3的食盐,但不能多吃,多吃会导致升高血压,促进动脉粥样硬化,故C错误;
D.在AgCl溶液中存在AgCl(s)?Ag+(aq)+Cl-(aq),饱和食盐水中c(Cl-)较大,相对蒸馏水来说,抑制AgCl的溶解,从而减小了AgCl的溶解,所以AgCl在蒸馏水中的溶解大于在饱和食盐水中的溶解度,故D错误;
故选B.
B.二氧化碳在水中溶解度较小,但是在碱性环境条件下溶解性很大,所以在侯氏制碱法中应该先通入氨气然后再通入二氧化碳,故B正确;
C.碘是人体必需微量元素,所以要吃富含KIO3的食盐,但不能多吃,多吃会导致升高血压,促进动脉粥样硬化,故C错误;
D.在AgCl溶液中存在AgCl(s)?Ag+(aq)+Cl-(aq),饱和食盐水中c(Cl-)较大,相对蒸馏水来说,抑制AgCl的溶解,从而减小了AgCl的溶解,所以AgCl在蒸馏水中的溶解大于在饱和食盐水中的溶解度,故D错误;
故选B.
点评:本题考查了化学与生活以及影响沉淀溶解平衡的因素,明确侯氏制碱法的原理以及沉淀溶解平衡的影响因素是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
能正确表示下列反应的离子方程式是( )
| A、Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O | ||
| B、等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-=Mg(OH)2↓ | ||
| C、将过量的SO2通入Ca(ClO)2溶液中:SO2+ClO-+H2O=HClO+HSO3- | ||
D、将0.2 mol?L-1的NH4Al(SO4)2溶液与0.3 mol?L-1的Ba(OH)2溶液等体积混合:2Al3++3SO
|
实验室中配制250mL 0.10mo1?L-1 NaOH溶液时,必须使用到的玻璃仪器是( )
A、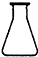 锥形瓶 |
B、 试管 |
C、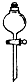 分液漏斗 |
D、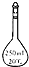 容量瓶 |
取等质量的碳酸钠(a)和碳酸钠与碳酸氢钠的混合物(b)分别进行下述实验,得出的结果正确的是( )
| A、与足量盐酸完全反应时,b耗酸量多 |
| B、与足量盐酸完全反应时,a产生二氧化碳多 |
| C、溶于水后分别加入足量澄清石灰水,b得到的沉淀量多 |
| D、配成等体积的溶液,b溶液中的c(Na+)大 |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、25℃、101.3kPa时,11.2L H2中含有的原子数为NA |
| B、14g N2中含有的原子数为NA |
| C、标准状况下,54mL H2O中含有的分子数为3NA |
| D、2L 1mol/L Na2SO4溶液中离子总数为3NA |
下列实验装置(固定装置略去)和操作正确的是( )
A、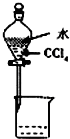 分离CCl4和水 |
B、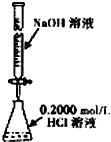 酸碱中和滴定 |
C、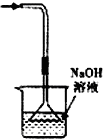 吸收HCl尾气 |
D、 中和热的测定 中和热的测定 |
下列混合物的分离和提纯方法中,主要是从沸点的角度考虑的是( )
| A、分液 | B、蒸馏 | C、过滤 | D、萃取 |