题目内容
15.在密闭容器中,将2.0mol CO与10mol H2O混合加热到800℃,达到下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g) K=1.0 则CO转化为CO2的转化率( )| A. | 83% | B. | 17% | C. | 50% | D. | 60% |
分析 设转化的CO为x,则
CO(g)+H2O(g)?CO2(g)+H2(g)
开始 2 10 0 0
转化 x x x x
平衡 2-x 10-x x x
$\frac{\frac{x}{V}×\frac{x}{V}}{\frac{(2-x)}{V}×\frac{(10-x)}{V}}$=1.0,以此来解答.
解答 解:设转化的CO为x,则
CO(g)+H2O(g)?CO2(g)+H2(g)
开始 2 10 0 0
转化 x x x x
平衡 2-x 10-x x x
$\frac{\frac{x}{V}×\frac{x}{V}}{\frac{(2-x)}{V}×\frac{(10-x)}{V}}$=1.0,解得x=1.66mol,
则CO转化为CO2的转化率为$\frac{1.66mol}{2mol}$×100%=83%,
故选A.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、K及转化率的计算为解答的关键,侧重分析与计算能力的考查,注意结合平衡浓度计算K,题目难度不大.

练习册系列答案
相关题目
6.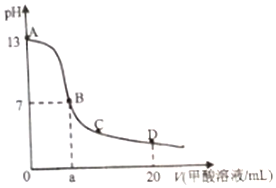 在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
 在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )| A. | 在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 | |
| B. | 在A、B间任意一点,c(HCOO-)>c(K+)>c(OH-)>c(H+) | |
| C. | 在D点:c(HCOO-)+c(HCOOH)>2c(K+) | |
| D. | B→C段:水的电离程度先增大后减小 |
10.等物质的量的下列化合物与足量浓盐酸反应,得到氯气的物质的量最多的是( )
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
7.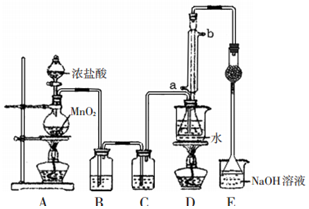 S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
已知:S2Cl2易与水反应.
下列是几种物质的熔沸点.
(1)写出装置A中制备Cl2的化学反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)装置B中盛放试剂的作用是吸收Cl2中的HCl气体; 装置C中的试剂是浓硫酸.
(3)D装置中采用水浴加热的优点是受热均匀,温度易控制; 反应结束后,从D装置锥形瓶内的混合物中分离出产物S2Cl2的实验方法是蒸馏.
(4)装置E中倒扣漏斗的作用是防止倒吸.
(5)S2Cl2易与水反应,有淡黄色沉淀生成,产生的无色气体能使品红溶液褪色,写出该反应的化学方程式2S2Cl2+2H2O=3S↓+SO2↑+4HCl.
 S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).已知:S2Cl2易与水反应.
下列是几种物质的熔沸点.
| 物质 | 沸点/℃ | 熔点/℃ |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)装置B中盛放试剂的作用是吸收Cl2中的HCl气体; 装置C中的试剂是浓硫酸.
(3)D装置中采用水浴加热的优点是受热均匀,温度易控制; 反应结束后,从D装置锥形瓶内的混合物中分离出产物S2Cl2的实验方法是蒸馏.
(4)装置E中倒扣漏斗的作用是防止倒吸.
(5)S2Cl2易与水反应,有淡黄色沉淀生成,产生的无色气体能使品红溶液褪色,写出该反应的化学方程式2S2Cl2+2H2O=3S↓+SO2↑+4HCl.
4.下列说法正确的是( )
| A. | 纤维素与淀粉互为同分异构体 | |
| B. | 糖类、油脂、蛋白质都是高分子化合物,一定条件下均能水解 | |
| C. | 煤的气化、煤的液化和石油的分馏都是化学变化 | |
| D. | 葡萄糖和蔗糖都含有C、H、O三种元素,但不是同系物 |
5.下列物质在光照时不反应的是( )
| A. | 氢气和氯气的混合气体 | B. | 硝酸 | ||
| C. | 氢气和氧气的混合气体 | D. | 氯水 |