题目内容
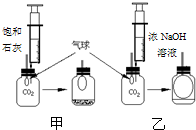 发现问题:研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液.
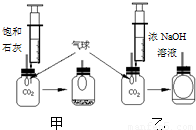
发现问题:研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液. 实验探究:在体积相同盛满CO2 的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH 溶液.实验装置和现象如图所示.请你一起参与.
现象结论:甲装置中产生的实验现象(用化学方程式表示)
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
,解释通常用石灰水而不用NaOH 溶液检验CO2的原因CO2与石灰水作用有明显实验现象,NaOH无明显现象
CO2与石灰水作用有明显实验现象,NaOH无明显现象
;乙装置中的实验现象是气球体积增大,溶液不变浑浊
气球体积增大,溶液不变浑浊
,吸收CO2较多的装置是乙
乙
.计算验证:另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2 应该用饱和石灰水.
思考评价:请你对小李同学的结论进行评价:
不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中
溶质的质量分数很小.
溶质的质量分数很小.
不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中
溶质的质量分数很小.
.溶质的质量分数很小.
分析:现象结论:根据甲装置中产生的实验现象出现白色沉淀,说明通常用饱和石灰水检验CO2;由反应现象知:甲、乙两装置的气球,乙的气球变化大,说明瓶内压强小,二氧化碳被吸收的多;
计算验证:小李同学的结论不正确,考虑Ca(OH)2微溶于水,而NaOH易溶于水,Ca(OH)2的饱和溶液远没有等质量的NaOH的饱和溶液含溶质的质量多;
计算验证:小李同学的结论不正确,考虑Ca(OH)2微溶于水,而NaOH易溶于水,Ca(OH)2的饱和溶液远没有等质量的NaOH的饱和溶液含溶质的质量多;
解答:解:现象结论:根据甲乙装置中产生的实验现象甲装置中石灰水变浑浊,乙装置中无现象,二氧化碳与澄清的石灰水反应生成碳酸钙沉淀,通过这一现象,可以用澄清的石灰水来检验二氧化碳的存在,方程式为CO2+Ca(OH)2=CaCO3↓+H2O;比较甲、乙两装置的实验现象可以看出,乙中气球变化大,说明瓶内压强小,二氧化碳被吸收的多,则吸收CO2的量甲<乙;
故答案为:CO2+Ca(OH)2=CaCO3↓+H2O;CO2与石灰水作用有明显实验现象,NaOH无明显现象;气球体积增大,溶液不变浑浊;乙;
思考评价:另一位同学小李同学通过计算结果发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2应该用饱和石灰水,小张的结论不正确.尽管理论上Ca(OH)2比等质量的NaOH吸收的CO2多,但由于Ca(OH)2微溶于水,而NaOH易溶于水,Ca(OH)2的饱和溶液远没有等质量的NaOH的饱和溶液含溶质的质量多,因此也没有NaOH的饱和溶液吸收CO2 的质量多,所以应用NaOH溶液吸收,
故答案为:不正确; 因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中溶质的质量分数很小.
故答案为:CO2+Ca(OH)2=CaCO3↓+H2O;CO2与石灰水作用有明显实验现象,NaOH无明显现象;气球体积增大,溶液不变浑浊;乙;
思考评价:另一位同学小李同学通过计算结果发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2应该用饱和石灰水,小张的结论不正确.尽管理论上Ca(OH)2比等质量的NaOH吸收的CO2多,但由于Ca(OH)2微溶于水,而NaOH易溶于水,Ca(OH)2的饱和溶液远没有等质量的NaOH的饱和溶液含溶质的质量多,因此也没有NaOH的饱和溶液吸收CO2 的质量多,所以应用NaOH溶液吸收,
故答案为:不正确; 因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中溶质的质量分数很小.
点评:本题考查了二氧化碳的检验,掌握酸碱盐的溶解性是解答的关键,题目难度中等.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目



 发现问题:研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液.
发现问题:研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液.