题目内容
20.A、B、C、D、E、F为6种短周期主族元素,它们的核电荷数依次递增,已知:B原子核外最外层电子数是次外层电子数的两倍,电子总数是E原子电子总数的$\frac{1}{2}$,F是同周期元素中原子半径最小的元素:D2-与E2+的电子层结构相同.B与D可以形成三原子化合物甲;A是非金属元素,且A、C、F可形成离子化合物乙.请回答:(1)F元素的名称是氯,E的元素符号是Mg.
(2)写出化合物乙的电子式
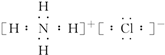 .
.(3)化合物甲有2个σ键,2个π键.
(4)B、C、D三种元素组成的气态氢化物的稳定性由强到弱的顺序是H2O>NH3>CH4.
分析 A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增.B原子核外最外层电子数是次外层电子数的两倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;B原子电子总数是E原子总数的$\frac{1}{2}$,则E原子核外电子数为12,故E为Mg;由原子序数可知,F处于第三周期,F是同周期元素中原子半径最小的元素,故F为Cl;D2-与E2+的电子层结构相同,离子核外电子数为10,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B与D可以形成三原子化合物甲为CO2;A是非金属元素,且A、C、F可形成离子化合物乙,则A为H元素,乙为NH4Cl,据此解答.
解答 解:A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增.B原子核外最外层电子数是次外层电子数的两倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;B原子电子总数是E原子总数的$\frac{1}{2}$,则E原子核外电子数为12,故E为Mg;由原子序数可知,F处于第三周期,F是同周期元素中原子半径最小的元素,故F为Cl;D2-与E2+的电子层结构相同,离子核外电子数为10,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B与D可以形成三原子化合物甲为CO2;A是非金属元素,且A、C、F可形成离子化合物乙,则A为H元素,乙为NH4Cl.
(1)F为氯元素,E为Mg元素,故答案为:氯、Mg;
(2)化合物乙为NH4Cl,电子式为: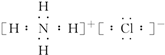 ,故答案为:
,故答案为: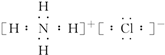 ;
;
(3)化合物甲为CO2,结构式为O=C=O,有2个σ键、2个π键,故答案为:2;2;
(4)非金属性O>N>C,故氢化物稳定性:H2O>NH3>CH4,故答案为:H2O>NH3>CH4.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解应用,有利于基础知识的巩固.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案| A. | 46g NO2和N2O4混合气体中含有原子数为3NA | |
| B. | 1mol Na2O2和Na2O中离子总数均为2NA | |
| C. | 1mol Mg与足量O2或N2反应均失去2NA个电子 | |
| D. | 标准状况下22.4L H2含有NA个分子 |
| A. | 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 标准状况下,2.24L NO和2.24L O2混合后气体分子数为0.15 NA | |
| C. | 加热条件下,1mol Fe投入足量的浓硫酸中,生成NA个SO2分子 | |
| D. | 0.1mol Na2O2与足是的潮湿的二氧化碳反应转移的电子数为0.1NA |
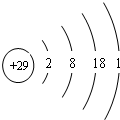
| 元素 | 结构或性质信息 |
| X | 其原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M | 单质在常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
| Q | 其与X形成的合金为目前用量最多的金属材料 |
 .
.(2)比较Y元素与氧元素的第一电离能大小顺序N>O;X和Z形成的化合物XZ2为一种液体溶剂,其电子式为
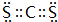 .
.(3)写出实验室制备M单质的离子方程式:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比稳定性强的是HF>HCl (写化学式):
| A. | O2分子间存在着非极性共价键 | |
| B. | CO2分子内存在着极性共价键 | |
| C. | SO2与H2O反应的产物是离子化合物 | |
| D. | 盐酸中含有H+和Cl-,故HCl为离子化合物 |
| A. | 食盐水 | B. | 干冰 | C. | 氯水 | D. | 浓硝酸 |

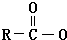 Na+NaOH$→_{△}^{CaO}$R-H+Na2CO3
Na+NaOH$→_{△}^{CaO}$R-H+Na2CO3 ,K的结构简式为
,K的结构简式为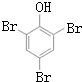 .
.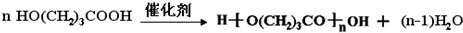 ;
;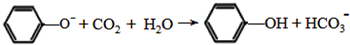 .
. (写结构简式).
(写结构简式).