题目内容
0.5mol C2H4与Cl2完全加成,再与Cl2彻底取代,两过程共用Cl2( )
| A、1mol | B、2mol |
| C、2.5mol | D、3mol |
考点:化学方程式的有关计算,取代反应与加成反应
专题:计算题
分析:乙烯与Cl2完全加成时,双键与Cl2的物质的量之比为1:1;1,2-二氯乙烷发生取代反应时,氢原子与Cl2的物质的量之比为1:1.
解答:
解:乙烯与Cl2完全加成时,双键与Cl2的物质的量之比为1:1,0.5molC2H4中双键的物质的量为0.5mol,所以0.5molC2H4与Cl2完全加成需要氯气的物质的量为0.5mol;
根据碳原子守恒知,生成1,2-二氯乙烷的物质的量为0.5mol,1,2-二氯乙烷发生取代反应时,氢原子与Cl2的物质的量之比为1:1,0.5mol1,2-二氯乙烷中氢原子的物质的量为2mol,所以发生取代反应需要氯气的物质的量为2mol,
通过以上分析知,需要氯气的物质的量=0.5mol+2mol=2.5mol,
故选C.
根据碳原子守恒知,生成1,2-二氯乙烷的物质的量为0.5mol,1,2-二氯乙烷发生取代反应时,氢原子与Cl2的物质的量之比为1:1,0.5mol1,2-二氯乙烷中氢原子的物质的量为2mol,所以发生取代反应需要氯气的物质的量为2mol,
通过以上分析知,需要氯气的物质的量=0.5mol+2mol=2.5mol,
故选C.
点评:本题以取代反应、加成反应为载体考查了物质的量的计算,根据双键和氯气、氢原子和氯气的关系式进行解答即可,难度中等.

练习册系列答案
相关题目
下列有关表述正确的是( )
| A、-OH与OH-组成元素相同,含有的质子数也相同 |
B、NH4Cl的电子式为: |
C、丙烷分子的比例模型示意图: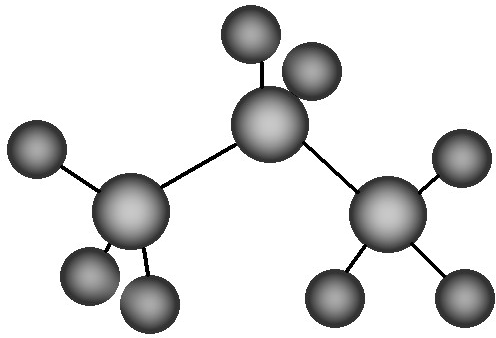 |
D、CO2分子的比例模型示意图: |
对于难溶盐MX,其饱和溶液的Mn+和Xn-离子的物质的量浓度之间的关系近似于水的离子积Kw(Kw=c(OH-) c(H+)),存在着c(Mn+) c(Xn-)=K的关系(K为常数).现将足量的AgCl固体分别放入下列物质中:
①10mL蒸馏水 ②40mL 0.03mol/L盐酸
③50mL 0.05mol/LAgNO3溶液 ④30mL 0.02mol/LCaCl2溶液
AgCl的溶解度由大到小排列的顺序是( )
①10mL蒸馏水 ②40mL 0.03mol/L盐酸
③50mL 0.05mol/LAgNO3溶液 ④30mL 0.02mol/LCaCl2溶液
AgCl的溶解度由大到小排列的顺序是( )
| A、①>②>④>③ |
| B、②>③>④>① |
| C、①>②>③>④ |
| D、③>②>④>① |
X、Y、Z、W、R、Q是6种短周期主族元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R、Q处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法不正确的是( )
| A、同周期元素的离子中W离子半径最小 |
| B、元素X能与元素Y形成共价化合物X2Y2 |
| C、工业上用二氧化锰和浓盐酸制取Q的单质 |
| D、元素Z、W、R的最高价氧化物对应的水化物之间均能反应 |
在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+对于该平衡,下列叙述正确的是( )
| A、加入少量CH3COONa固体,平衡向逆向移动,溶液导电能力增强 | ||
| B、加入少量NaOH固体,平衡向正向移动,溶液中c(H+)增大 | ||
C、加水,平衡向正向移动,
| ||
| D、通入少量HCl气体,平衡逆向移动,溶液中c(H+)减少 |
下列溶液中有关物质的量浓度关系正确的是( )
| A、Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③ |
| C、NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
| D、0.1mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
下列过程或现象与盐类水解无关的是( )
| A、硫化钠浓溶液有臭味 |
| B、加热氯化铁溶液颜色变深 |
| C、铁在潮湿的环境下生锈 |
| D、纯碱溶液去油污 |
 2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.


