题目内容
将2 mol NaHCO3和一定量的Na2O2固体混合,在加热的条件下使其反应,经测定无Na2O2剩余,则最后所得固体的物质的量(n)为( )
| A.1mol<n≤2mol | B.1mol<n≤4mol |
| C.2mol<n≤4mol | D.n>4mol |
B
解析试题分析:采用极值法进行计算,Na2O2最小值的极限为0,2 mol NaHCO3分解生成1mol Na2CO3;Na2O2最大值为恰好与2mol NaHCO3分解产生的CO2、H2O完全反应,1mol二氧化碳和过氧化钠反应生成1mol碳酸钠,1mol水和过氧化钠反应生成2mol氢氧化钠,再加上2 mol NaHCO3分解生成的1mol Na2CO3,则最后所得固体的物质的量为4mol。故B项正确。
考点:本题考查极值法和根据化学方程式的计算。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
下列关于钠的叙述中,不正确的是
| A.钠燃烧时发出黄色的火焰 | B.钠燃烧时生成氧化钠 |
| C.钠有很强的还原性 | D.钠原子的最外层只有一个电子 |
向含n mol 硫酸铝的溶液中加入m mol NaOH溶液,观察到的现象是先有白色沉淀生成,后部分溶解,则生成Al(OH)3沉淀的物质的量是
| A.(8n-m)mol | B.(4m-n)mol | C.(4n-m)mol | D.(7n-m)mol |
在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质:①FeCl3;②Fe2O3;③Cu(NO3)2;④KNO3,铜粉溶解的是( )
| A.只有①或② |
| B.只有①或②或④ |
| C.只有①或②或③ |
| D.上述任意一种 |
下列现象或反应的原理解释正确的是
| | 现象或反应 | 原理解释 |
| A. | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔对熔化的铝有较强的吸附作用 |
| B. | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
| C. | 镀层破损后,镀锡铁比镀锌铁易腐蚀 | 锡比锌活泼 |
| D. | 2CO=C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S<0 |
现有一块已知质量的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案
实验设计1:铝镁合金 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计2:铝镁合金 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计3:铝镁合金 溶液
溶液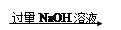 过滤,测定得到沉淀的质量
过滤,测定得到沉淀的质量
则能测定出镁的质量分数的是( )
| A.都能 | B.都不能 | C.①不能,其它都能 | D.②③不能,①能 |
下列物质的保存方法正确的是:
| A.氢氧化钠溶液可盛放在带橡皮塞的玻璃瓶中 |
| B.氢氧化钠溶液可盛放在带玻璃塞的玻璃瓶中 |
| C.单质钠贮存在水中 |
| D.氢氧化钠可以长久露置在空气中存放 |