题目内容
9.将20.0g NaOH固体溶于水配成100mL溶液.(1)该溶液中NaOH的物质的量浓度为5mol/L.
(2)从该溶液中取出10mL,其中NaOH的物质的量浓度为5mol/L,含NaOH的质量为2.0g.
(3)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为0.5mol/L.
分析 (1)根据n=$\frac{m}{M}$计算出氢氧化钠的物质的量,再根据c=$\frac{n}{V}$计算出该氢氧化钠溶液的浓度;
(2)溶液具有均一性,取出的溶液浓度不变;根据m=cVM计算取出溶液中含有氢氧化钠的质量;
(3)稀释过程中氢氧化钠的物质的量不变,据此计算出稀释后氢氧化钠的浓度.
解答 解:(1)20.0g氢氧化钠的物质的量为:$\frac{20.0g}{40g/mol}$=0.5mol/L,该氢氧化钠溶液的浓度为$\frac{0.5mol}{0.1L}$=5mol/L,
故答案为:5mol/L;
(2)从该溶液中取出10mL,溶液具有均一性,则取出的NaOH溶液的物质的量浓度仍然为5mol/L,含NaOH的质量为:40g/mol×5mol/L×0.01L=2.0g,
故答案为:5mol/L;2.0g;
(3)将取出的10mL溶液加水稀释到100mL,稀释过程中氢氧化钠的物质的量不变,则稀释后溶液中NaOH的物质的量浓度为$\frac{5mol/L×0.01L}{0.1L}$=0.5mol/L,
故答案为:0.5mol/L.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的表达式为解答关键,注意掌握物质的量与摩尔质量、物质的量浓度之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
17.下列液体中,不会出现丁达尔效应的分散系是( )
①鸡蛋白溶液;②淀粉溶液;③硫酸钠溶液;④纯水;⑤沸水中滴入饱和FeCl3溶液;⑥肥皂水;⑦把氯化钠研磨成直径在1~100nm的颗粒然后分散于水中.
①鸡蛋白溶液;②淀粉溶液;③硫酸钠溶液;④纯水;⑤沸水中滴入饱和FeCl3溶液;⑥肥皂水;⑦把氯化钠研磨成直径在1~100nm的颗粒然后分散于水中.
| A. | ③⑦ | B. | ③④⑦ | C. | ②④ | D. | ③④ |
4.0.2mol CH4的质量为( )
| A. | 1.6 g | B. | 3.2 g | C. | 5.6 g | D. | 8 g |
14.食盐、纯碱(Na2CO3)、食醋均为厨房中常用的物质,利用这些物质不能实现的实验是( )
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①② |
1.下列说法错误的是( )
| A. | 摩尔是物质的量的单位 | |
| B. | 国际上规定,0.012kg 12C原子所含有的碳原子数目的物质的量为1mol | |
| C. | mol H2的质量是2g,它所占的体积是 22.4L | |
| D. | 硫酸根离子的摩尔质量是 96g/mol |
12.1g N2中含有x个原子,则阿伏加德罗常数的值是( )
| A. | $\frac{x}{28}$mol-1 | B. | $\frac{x}{14}$mol-1 | C. | 14x mol-1 | D. | 28x mol-1 |
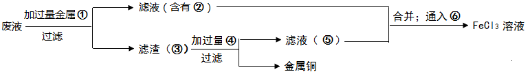
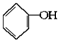 合成
合成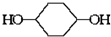 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).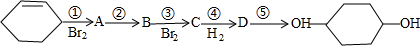
 、D
、D .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ .
.