题目内容
在下列物质中,化合物类型相同的一组是( )
| A、NaCl HCl |
| B、CO2 H2O |
| C、H2CO3 KCl |
| D、MgCl2 SO2 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物可能含有共价键,只含共价键的化合物是共价化合物,共价化合物一定不含离子键,据此分析解答.
解答:
解:A.NaCl中Na和Cl元素之间以离子键结合,HCl中Cl和H元素之间以共价键结合,所以两物质含有的化学键类型不同,故A错误;
B.CO2 分子中C元素和O元素之间以共价键结合,H2O中H元素和O元素之间以共价键结合,所以CO2和H2O所含的化学键类型相同,故B正确;
C.H2CO3中元素之间以共价键结合,KCl中Cl元素和K元素之间以离子键结合,所以两物质含有的化学键类型不同,故C错误;
D.MgCl2中Cl元素和Mg元素之间以离子键结合,SO2中S元素和O元素之间以共价键结合,所以两物质含有的化学键类型不同,故D错误;
故选B.
B.CO2 分子中C元素和O元素之间以共价键结合,H2O中H元素和O元素之间以共价键结合,所以CO2和H2O所含的化学键类型相同,故B正确;
C.H2CO3中元素之间以共价键结合,KCl中Cl元素和K元素之间以离子键结合,所以两物质含有的化学键类型不同,故C错误;
D.MgCl2中Cl元素和Mg元素之间以离子键结合,SO2中S元素和O元素之间以共价键结合,所以两物质含有的化学键类型不同,故D错误;
故选B.
点评:本题考查了化学键类型的判断,难度不大,注意金属元素和非金属元素之间存在的化学键不一定是离子键,如氯化铝中氯元素和铝元素之间以共价键结合.

练习册系列答案
相关题目
需加入适当的氧化剂才能实现的反应是( )
| A、PCl5→PCl3 |
| B、MnO2→Mn2+ |
| C、SO2→SO32- |
| D、Fe→Fe2O3 |
下列判断不合理的是( )
| A、能电离出H+的物质一定是酸 |
| B、焰色反应是物理变化 |
| C、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
| D、蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
下列变化中不需要破坏化学键的是( )
| A、加热氯化铵 |
| B、干冰气化 |
| C、熔融氯化钠导电 |
| D、氯化氢溶于水 |
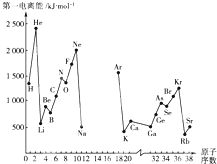 根据信息回答列问题:
根据信息回答列问题: