题目内容
2.已知反应:①2H2O(g)=2H2(g)+O2(g)△H1
②Cl2(g)+H2(g)=2HCl△H2
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3
则△H1、△H2、△H3间的关系正确的是( )
| A. | △H1+△H2=△H3 | B. | △H1-△H2=△H3 | C. | △H1+2△H2=△H3 | D. | △H1-2△H2=△H3 |
分析 根据盖斯定律将①+②×2可得:③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g),据此分析△H1、△H2、△H3间的关系.
解答 解:已知反应:①2H2O(g)=2H2(g)+O2(g)△H1
②Cl2(g)+H2(g)=2HCl△H2
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3,
根据盖斯定律将①+②×2可得:③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3=△H1+2△H2,
故选C.
点评 本题考查盖斯定律在反应热中的计算,题目难度不大,明确盖斯定律的内容为解答关键,注意掌握化学反应与能量变化的关系,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
13.有四种短周期的主族元素X、Y、Z、W.X的一种原子常用于鉴定文物的年代,Y是地壳中含量最多的金属元素,W的原子核外某两层电子数目之比为4:3,X和Z同族.下列说法中正确的是( )
| A. | 简单离子半径:Y>W | |
| B. | 上述四种元素的单质中只有2种能导电 | |
| C. | X与Z两者的最高价氧化物的组成和结构相似 | |
| D. | 在加热条件下,Y的单质可溶于W的最高价含氧酸的浓溶液中 |
14.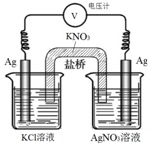 一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
 一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 右池中的银电极作负极 | B. | 总反应为Ag++Cl-=AgCl | ||
| C. | 正极反应为Ag-e-=Ag+ | D. | 盐桥中的NO3-向右池方向移动 |
11.水是自然界最重要的分散剂,关于水的叙述错误的是( )
| A. | 水分子是含极性键的极性分子 | |
| B. | 水的电离方程式为:H2O?2H++O2- | |
| C. | 重水(D2O)分子中,各原子质量数之和是质子数之和的两倍 | |
| D. | 相同质量的水具有的内能:固体<液体<气体 |
18.下列试剂中,可以鉴别二氧化碳和二氧化硫的是( )
| A. | 澄清石灰水 | B. | 品红溶液 | ||
| C. | 湿润的蓝色石蕊试纸 | D. | 硝酸银溶液 |
14.下列各组物质发生化学反应时,由于反应物的量不同而生成不同产物的是( )
①CO2与NaOH溶液
②NaHCO3溶液与盐酸
③Na与氧气
④C与O2
⑤AlCl3溶液与氨水
⑥Fe与Cl2.
①CO2与NaOH溶液
②NaHCO3溶液与盐酸
③Na与氧气
④C与O2
⑤AlCl3溶液与氨水
⑥Fe与Cl2.
| A. | ①③④⑥ | B. | ①④⑥ | C. | ①④ | D. | ①③④ |
11.25℃时,下列各组离子在指定溶液中可能大量共存的是( )
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | 无色溶液中:Cu2+、Al3+、NH4+、Cl- | |
| C. | 由水电离出的c(H+)=1×10-13mol•L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| D. | 0.1mol•L-1FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
12.下列有关化学反应过程或实验现象的叙述中,正确的是( )
| A. | 氯气的水溶液可以导电,说明氯气是电解质 | |
| B. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| C. | 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 | |
| D. | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,说明BaCl2溶液具有酸性 |
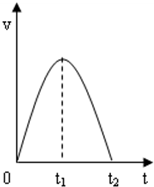 (1)将粉末形状大小相同的铁和铝分别与等浓度的稀盐酸反应产生气泡的速率铝>铁(填“<、>、=”).Al与盐酸反应的离子方程式是2Al+6H+=2Al3++3H2↑.
(1)将粉末形状大小相同的铁和铝分别与等浓度的稀盐酸反应产生气泡的速率铝>铁(填“<、>、=”).Al与盐酸反应的离子方程式是2Al+6H+=2Al3++3H2↑.