题目内容
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρ g·cm3,质量分数为w,其中含NH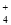 的物质的量为b mol。下列叙述中不正确的( )。
的物质的量为b mol。下列叙述中不正确的( )。
A.溶质的质量分数w= ×100%
×100%
B.溶质的物质的量浓度c=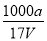 mol·L-1
mol·L-1
C.溶液中c(OH-)=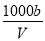 mol·L-1+c(H+)
mol·L-1+c(H+)
D.上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5 w
A
【解析】
试题分析:A.溶质的质量分数w=[m(质)÷m(剂)]×100%=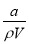 ×100%,错误;B.溶质的物质的量浓度c=
×100%,错误;B.溶质的物质的量浓度c= =
=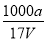 mol·L-1,正确;C.根据溶液呈电中性原则可知:溶液中c(OH-)=c(NH
mol·L-1,正确;C.根据溶液呈电中性原则可知:溶液中c(OH-)=c(NH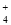 ) +c(H+)=
) +c(H+)=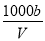 mol·L-1+c(H+),正确;D.将上述溶液中再加入V mL水后,由于氨水与水混合后溶液的体积小于各种物质的溶液的体积和,在稀释过程中溶质的质量不变,所以所以溶液稀释后的密度比原来大,因此所得溶液中溶质的质量分数小于0.5 w,正确。
mol·L-1+c(H+),正确;D.将上述溶液中再加入V mL水后,由于氨水与水混合后溶液的体积小于各种物质的溶液的体积和,在稀释过程中溶质的质量不变,所以所以溶液稀释后的密度比原来大,因此所得溶液中溶质的质量分数小于0.5 w,正确。
考点:考查溶液的质量分数、物质的量浓度的计算及溶液稀释中两种浓度的大小比较及质量发生的计算。

下列实验方案中,不能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |

 2C
2C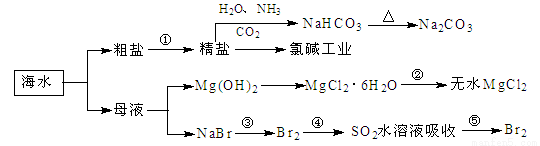
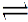 ?H2(g)+
?H2(g)+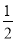 S2(g)
S2(g)