题目内容
下列除去杂质(试样中括号内的物质是杂质)时,选用的试剂正确的是( )
| A | B | C | D | |
| 试样 | Na2CO3(NaHCO3) | FeCl2(FeCl3) | Fe(A1) | Cl2(HCl) |
| 除杂试剂 | 澄清石灰水 | NaOH溶液 | NaOH溶液 | 饱和NaHCO3溶液 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:A.Na2CO3和NaHCO3都与澄清石灰水反应;
B.二者都与氢氧化钠溶液反应;
C.铝和与氢氧化钠溶液反应;
D.氯气和水反应生成盐酸和次氯酸,可与NaHCO3溶液反应.
B.二者都与氢氧化钠溶液反应;
C.铝和与氢氧化钠溶液反应;
D.氯气和水反应生成盐酸和次氯酸,可与NaHCO3溶液反应.
解答:
解:A.Na2CO3和NaHCO3都与澄清石灰水反应,应用加热的方法除杂,故A错误;
B.二者都与氢氧化钠溶液反应,可加入铁除杂,故B错误;
C.铝和氢氧化钠溶液反应,而铁不反应,可除杂,故C正确;
D.氯气和水反应生成盐酸和次氯酸,可与NaHCO3溶液反应,应用饱和食盐水,故D错误.
故选C.
B.二者都与氢氧化钠溶液反应,可加入铁除杂,故B错误;
C.铝和氢氧化钠溶液反应,而铁不反应,可除杂,故C正确;
D.氯气和水反应生成盐酸和次氯酸,可与NaHCO3溶液反应,应用饱和食盐水,故D错误.
故选C.
点评:本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意除杂时不能引入新杂质,更不能影响被提纯物质的性质,难度不大.

练习册系列答案
相关题目
反应:aX(g)+bY(g)?cZ(g),达到平衡时测得X气体的浓度为1mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为0.6mol/L,则下列叙述正确的是( )
| A、a+b<c |
| B、平衡向生成Z的方向移动 |
| C、Z的体积分数降低 |
| D、Y的转化率升高 |
下列实验操作或有关叙述正确的是( )
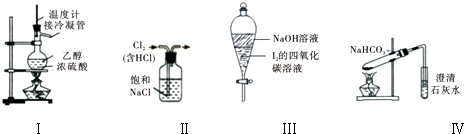

| A、用装置Ⅰ在实验室制备少量乙烯 |
| B、用装置Ⅱ来除去氯气中含有的HCl气体 |
| C、装置Ⅲ中,充分振荡后静置,下层溶液颜色保持不变 |
| D、用装置Ⅳ来探究NaHCO3的热稳定性 |
已知如下两个热化学反应方程式:下列说法错误的是( )
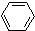 (1)+H2(g)→
(1)+H2(g)→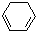 (1)-Q ①
(1)-Q ①
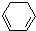 (1)+2H2(g)→
(1)+2H2(g)→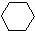 (1)+Q ②
(1)+Q ②
 (1)+H2(g)→
(1)+H2(g)→ (1)-Q ①
(1)-Q ① (1)+2H2(g)→
(1)+2H2(g)→ (1)+Q ②
(1)+Q ②| A、反应①、②都属于加成反应 |
| B、1,3-环己二烯比苯稳定 |
| C、反应①、②的热效应说明苯环中含有的并不是碳碳双键 |
| D、反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
下列提纯物质的实验方法不正确的是( )
①用Na2CO3溶液除去混在NaCl溶液中的MgCl2杂质
②用蒸馏法除去混在水中的氧气
③用酒精萃取溶解在水中的溴
④将KMnO4溶液减压低温蒸发,以获得晶体KMnO4.
①用Na2CO3溶液除去混在NaCl溶液中的MgCl2杂质
②用蒸馏法除去混在水中的氧气
③用酒精萃取溶解在水中的溴
④将KMnO4溶液减压低温蒸发,以获得晶体KMnO4.
| A、② | B、③④ |
| C、①②③ | D、①②③④ |
向一定量的Cu、Fe203的混合物中加人600mL 2mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,再加入过量1mol/L NaOH溶液,将沉淀过滤、洗涤、干燥,称得质量比原混合物增重17.6g,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量是( )
| A、4.8 g |
| B、8.8 g |
| C、9.6g |
| D、14.4g |
铁、铜混合粉末18.0g加入到100ml 5.0mol/LFeCl3溶液中,剩余固体质量为3.2g.下列说法正确的是( )
| A、剩余固体是铁、铜混合物 |
| B、原固体混合物中铜的质量是9.6g |
| C、反应后溶液中n(Fe3+)=0.10 mol |
| D、反应后溶液中n(Fe2+)+n(Cu2+)=0.75 mol |
化学反应中一定伴随着能量的变化,下列有关能量的说法错误的是( )
| A、水的电离是吸热过程 |
| B、任何中和反应都是放热反应 |
| C、电解饱和食盐水时,电能转变成化学能 |
| D、由2H2(g)+O2(g)?2H2O(g)△H=-483.6kj?mol-1,可知的燃烧热为241.8kJ?mol-1 |