题目内容
己知0.1mol/LNaHCO3溶液显碱性,将此溶液加水稀释后,下列说法正确的是( )
| A、稀释后,溶液中各离子浓度均变小 | ||||
| B、原溶液中,C(Na+)=C(HCO3-)+C(H2CO3)=0.1mol/L | ||||
C、稀释后,溶液中
| ||||
| D、原溶液加入少量NaOH溶液后,其碱性减弱 |
考点:盐类水解的原理
专题:
分析:A.溶液加水稀释,氢氧根离子浓度减小,则氢离子浓度增大;
B.根据物料守恒分析;
C.加水稀释,水解平衡H2O+HCO3-?OH-+H2CO3向正方向移动,根据物质的量变化分析;
D.加强碱,碱性增强.
B.根据物料守恒分析;
C.加水稀释,水解平衡H2O+HCO3-?OH-+H2CO3向正方向移动,根据物质的量变化分析;
D.加强碱,碱性增强.
解答:
解:A.溶液加水稀释,氢氧根离子浓度减小,由于Kw不变,则氢离子浓度增大,故A错误;
B.原溶液中,存在物料守恒:C(Na+)=C(HCO3-)+C(CO32-)+C(H2CO3)=0.1mol/L,故B错误;
C.加水稀释,水解平衡H2O+HCO3-?OH-+H2CO3向正方向移动,HCO3-的物质的量减小,Na+的物质的量不变,溶液中
=
,则比值增大,故C正确;
D.原溶液加入少量NaOH溶液,氢氧化钠与NaHCO3为暗反应生成碳酸钠,等浓度的碳酸钠的碱性大于碳酸氢钠,则其碱性增强,故D错误;
故选C.
B.原溶液中,存在物料守恒:C(Na+)=C(HCO3-)+C(CO32-)+C(H2CO3)=0.1mol/L,故B错误;
C.加水稀释,水解平衡H2O+HCO3-?OH-+H2CO3向正方向移动,HCO3-的物质的量减小,Na+的物质的量不变,溶液中
| C(Na+) | ||
C(HC
|
| n(Na+) |
| n(HCO3-) |
D.原溶液加入少量NaOH溶液,氢氧化钠与NaHCO3为暗反应生成碳酸钠,等浓度的碳酸钠的碱性大于碳酸氢钠,则其碱性增强,故D错误;
故选C.
点评:本题考查了盐类的水解,题目难度不大,根据“谁弱谁水解”、“谁强谁显性”来分析解答即可,注意把握影响盐类的水解平衡的因素.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、含氧酸的酸性:X对应的酸性强于Y对应的酸性 |
| B、第一电离能Y不一定小于X |
| C、X与Y形成化合物时,X显负价,Y显正价 |
| D、Y的气态氢化物的稳定性小于X气态氢化物的稳定性 |
下列说法中,错误的是( )
| A、向Na2SiO3溶液中通入CO2产生白色胶状沉淀 |
| B、NaOH溶液不能存放在磨口玻璃塞的试剂瓶中 |
| C、二氧化硅溶于水生成硅酸 |
| D、二氧化硅是一种熔沸点很高、硬度很大的氧化物 |
20°C时有ag硫酸铜溶液VmL.将溶液蒸发掉bg水后恢复到20°C,恰好全部生成硫酸铜晶体(CuSO4?5H2O),则下列关系式错误的是( )
A、原硫酸铜溶液的密度为ρ=
| ||
B、原硫酸铜溶液的物质的量浓度为c(CuSO4)=
| ||
C、原硫酸铜溶液的质量分数ω(CuSO4)=
| ||
D、生成硫酸铜晶体的物质的量为
|

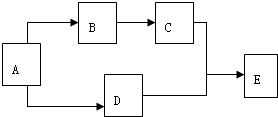 有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示.已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题:
有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示.已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题: