题目内容
13.如图是温度和压强对反应X+Y?2Z影响的示意图.下列叙述正确的是( )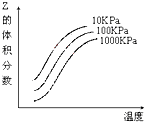
| A. | 上述可逆反应的正反应为放热反应 | B. | X、Y、Z均为气态 | ||
| C. | X和Y中只有一种是气态,Z为气态 | D. | 上述反应的正反应的△H>0 |
分析 由图象曲线变化可知,随着温度的升高,Z的体积分数增大,说明升高温度平衡向正反应方向移动,说明正反应吸热,增大压强,Z的体积分数减小,说明增大压强平衡向逆反应方向移动,则说明反应前的气体计量数之和小于生成物气体的化学计量数,以此解答该题.
解答 解:A.图象曲线变化可知,随着温度的升高,Z的体积分数增大,说明升高温度平衡向正反应方向移动,说明正反应吸热,故A错误;
B.如X、Y、Z均为气态,反应前后气体的体积不变,增大压强,平衡应不移动,但由图象可知增大压强平衡向逆反应方向移动,故B错误;
C.增大压强,Z的体积分数减小,说明增大压强平衡向逆反应方向移动,则说明反应前的气体计量数之和小于生成物气体的化学计量数,则X和Y中只有一种是气态,Z为气态,故C正确;
D.图象曲线变化可知,随着温度的升高,Z的体积分数增大,说明升高温度平衡向正反应方向移动,说明正反应吸热,正反应的△H>0,故D正确.
故选CD.
点评 本题考查化学平衡移动的图象问题,题目难度中等,解答该题的关键是把握图象中曲线的变化特点,结合外界条件对化学平衡的影响分析.

练习册系列答案
相关题目
3.下列溶液中能够区别SO2和CO2气体的是( )
①澄清石灰水 ②H2S溶液 ③KMnO4溶液 ④品红溶液.
①澄清石灰水 ②H2S溶液 ③KMnO4溶液 ④品红溶液.
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
8.下列说法或表示方法正确的是( )
| A. | 等质量的硫蒸气和硫磺分别完全燃烧,二者放出的热量一样多 | |
| B. | 氢气的燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-Q1 kJ/mol 2H2(g)+O2(g)═2H2O(g)△H=-Q2 kJ/mol,则Q1>Q2 | |
| D. | 已知中和热为57.3 kJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
5.SO2既有氧化性又有还原性,通常以还原性为主,Fe3+和Cr2O72-具有氧化性.将SO2与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,前后依次发生两个氧化还原反应.据此下列有关说法正确的是( )
| A. | 还原性:Cr3+>Fe2+>SO2 | |
| B. | 氧化性:Cr2O72->SO2>Fe3+ | |
| C. | 足量的SO2也不能使Fe2(SO4)3溶液完全褪去颜色 | |
| D. | Fe2(SO4)3在前一个反应中做氧化剂,后一个反应中做还原剂 |
2.已知反应H2(g)+Br2(g)=2HBr(g)△H=-83kJ•mol-1,1molH2(g)、1molBr2(g) 分子中化学键断裂时分别需要吸收436kJ、193kJ的能量,则断开1molHBr(g) 分子中化学键需吸收的能量为( )
| A. | 566kJ | B. | 283kJ | C. | 712kJ | D. | 356kJ |
3.“宽带中国”战略的阶段性发展目标指出,2015年要基本实现城市光纤到楼入户、农村宽带进乡入村,光纤到户(FTTH)要达0.7亿用户.光纤(光导纤维的简称)的主要成分是( )
| A. | 晶体硅 | B. | 二氧化硅 | C. | 硅酸钠 | D. | 铝硅合金 |
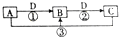 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下,它们之间的相互转化关系如图所示(反应中生成的H2O已略去).请回答下列问题:
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下,它们之间的相互转化关系如图所示(反应中生成的H2O已略去).请回答下列问题: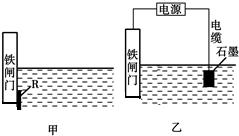 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一.
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一.