题目内容
下列反应中,SO2作还原剂的是( )
| A、2H2S+SO2→3S↓+2H2O |
| B、SO2+2Mg→2MgO+S |
| C、Cl2+SO2+2H2O→H2SO4+2HCl |
| D、SO2+2NaOH→Na2SO3+H2O |
考点:氧化还原反应
专题:
分析:在氧化还原反应中,二氧化硫作还原剂,则二氧化硫在反应中失电子化合价升高,以此解答该题.
解答:
解:A.该反应中,二氧化硫中硫元素得电子化合价降低,所以二氧化硫是氧化剂,故A错误;
B.反应中,S元素化合价降低,被还原,SO2为氧化剂,故B错误;
C.S元素化合价升高,被氧化,为还原剂,故C正确;
D.S元素化合价不变,不是氧化还原反应,故D错误.
故选C.
B.反应中,S元素化合价降低,被还原,SO2为氧化剂,故B错误;
C.S元素化合价升高,被氧化,为还原剂,故C正确;
D.S元素化合价不变,不是氧化还原反应,故D错误.
故选C.
点评:本题考查氧化还原反应,侧重于基本概念的理解和运用的考查,为高频考点,注意从元素化合价的角度解答该题,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
下列两分子的关系是( )
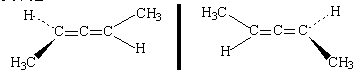
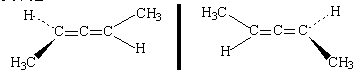
| A、互为同素形体 |
| B、同一物质 |
| C、手性异构体 |
| D、互为同系物 |
 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示.下列叙述错误的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示.下列叙述错误的是( )| A、x与y的差值为0.01mol |
| B、原溶液中c(Cl-)=0.85mol?L-1 |
| C、原溶液的c(H+)=0.1mol?L-1 |
| D、原溶液中n(Mg2+):n(Al3+)=5:1 |
用蒸馏水湿润过的pH试纸测得某氨基酸溶液的pH等于8,则该氨基酸溶液的pH可能是( )
| A、9 | B、8 | C、7 | D、6 |
加热升高温度时,化学反应速率加快,最主要原因是( )
| A、分子运动速率加快,使该反应物分子的碰撞机会增多 |
| B、反应物分子的能量增加,活化分子浓度增大,有效碰撞次数增多 |
| C、该化学反应的过程是吸热造成的 |
| D、该化学反应的过程是放热造成的 |
下列离子方程式中错误的是( )
| A、明矾净水的原理:Al3++3H2O=Al(OH)3↓+3H+ |
| B、硫酸铝溶液与硫化钠溶液混合:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑ |
| C、碳酸钠溶液呈碱性的原因:CO32-+2H2O?H2CO3+2OH- |
| D、FeCl3溶液加入碳酸氢钠溶液中:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑ |
钠元素在自然界存在的主要形式为( )
| A、金属钠 |
| B、NaOH |
| C、NaCl |
| D、Na2CO3 |