题目内容
在50mL 0.01mol?L-1下列溶液中,溶解CaCO3质量最大的是( )
| A、Na2CO3溶液 |
| B、NaOH溶液 |
| C、NH4Cl溶液 |
| D、NaHCO3溶液 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:饱和CaCO3溶液中存在,CaCO3(s)?Ca2+(aq)+CO32-(aq),溶液溶解CaCO3质量最大,则溶液可与Ca2+或CO32-反应,使平衡正向移动,以此解答该题.
解答:
解:饱和CaCO3溶液中存在,CaCO3(s)?Ca2+(aq)+CO32-(aq),
Na2CO3溶液和NaHCO3溶液存在CO32-,抑制CaCO3的溶解;
NaOH溶液对平衡移动基本没有影响;
NH4Cl溶液水解呈酸性,可与CO32-反应,进而促进CaCO3的溶解,
故选C.
Na2CO3溶液和NaHCO3溶液存在CO32-,抑制CaCO3的溶解;
NaOH溶液对平衡移动基本没有影响;
NH4Cl溶液水解呈酸性,可与CO32-反应,进而促进CaCO3的溶解,
故选C.
点评:本题考查难溶电解质的溶解平衡,为高频考点,侧重于学生的分析能力的考查,难度不大,注意从平衡移动的角度解答该题.

练习册系列答案
相关题目
芥子气[(ClCH2CH2)2S是一种毒气,即使嗅觉不能感受的极低浓度也会对人造成伤害,可用Na0H溶液解毒.芥子气可用以下方法制备 2CH2=CH2+S2Cl2→(ClCH2CH2)2S+S下列有关说法正确的是( )
| A、芥子气是直线型分子 |
| B、S2Cl2中有极性键和非极性键 |
| C、制备反应中S2Cl2,作还原剂 |
| D、NaOH溶液解毒原理是中和反应 |
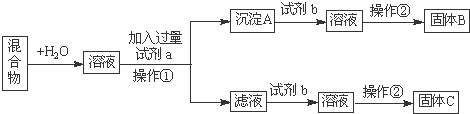
还原沉淀法是处理含铬(含Cr2072-和CrO42-)工业废水的常用方法,过程如下:CrO
Cr2O
Cr 3+
Cr(OH)3↓已知转化过程中的反应为:2CrO
(aq)+2H+ (aq)?Cr2O
(aq)+H2O(l).转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有
转化为Cr2072-,下列说法不正确的是( )
2- 4 |
| H+ |
| 转换 |
2- 7 |
| Fe2+ |
| 还原 |
| OH- |
| 沉淀 |
2- 4 |
2- 7 |
| 10 |
| 11 |
| A、溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B、若用绿矾(FeS04?7H20)(M=278)作还原剂,处理1 L废水,至少需要917.4 g |
| C、常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D、常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
在下列条件下能制得括号中物质的是( )
A、苯在常温下与浓硝酸混合(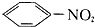 ) ) |
| B、将乙烯通入到水中(CH3CH2OH) |
C、甲苯与氯气在氯化铁催化下反应( ) ) |
| D、乙醇在银催化下加热与氧气反应(CH3CHO) |
为了除去混入CO2中的SO2,最好将混合气体通入下列哪种溶液中( )
| A、饱和烧碱溶液 |
| B、饱和小苏打溶液 |
| C、饱和纯碱溶液 |
| D、浓硫酸 |
 卡托普列(Captopril)临床用于治疗高血压和充血性心力衰竭.它最有价值的合成路线为:
卡托普列(Captopril)临床用于治疗高血压和充血性心力衰竭.它最有价值的合成路线为: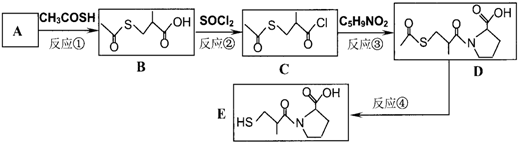
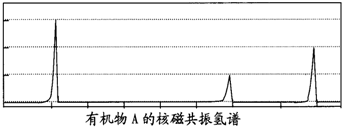
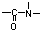 能在碱性条件下水解.则1molE最多能与
能在碱性条件下水解.则1molE最多能与