题目内容
10.下列有关离子浓度的判断正确的是( )| A. | 0.1 mol•L-1NaHCO3溶液中:c(Na+)=c(HCO3-)=0.1 mol•L-1 | |
| B. | 0.2 mol•L-1NaHS溶液和0.1 mol•L-1Na2S溶液等体积混合,混合液中:3c(Na+)=4c(H2S)+4c(HS-)+4c(S2-) | |
| C. | KAl(SO4)2的水溶液中:c(SO42-)>c(A13+)>c(K+)>c(H+)>c(OH-) | |
| D. | H2SO3溶液中:c(H+)=2c(SO32-)>c(OH-) |
分析 A.碳酸氢钠溶液中,碳酸氢根离子部分水解,导致碳酸氢根离子的浓度减小;
B.0.2 mol•L-1NaHS溶液和0.1 mol•L-1Na2S溶液等体积混合,根据混合液中的物料守恒判断;
C.铝离子部分水解,导致铝离子浓度减小,则c(K+)>c(A13+);
D.根据亚硫酸溶液中的电荷守恒分析.
解答 解:A.0.1 mol•L-1NaHCO3溶液中,碳酸氢根离子部分水解,则:c(Na+)=0.1 mol•L-1>c(HCO3-),故A错误;
B.0.2 mol•L-1NaHS溶液和0.1 mol•L-1Na2S溶液等体积混合,根据物料守恒可得:3c(Na+)=4c(H2S)+4c(HS-)+4c(S2-),故B正确;
C.KAl(SO4)2的水溶液中,铝离子部分水解,导致铝离子浓度减小,则c(K+)>c(A13+),正确的离子浓度大小为:c(SO42-)>c(K+)>c(A13+)>c(H+)>c(OH-),故C错误;
D.H2SO3溶液中,根据电荷守恒可知:c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),则c(H+)>2c(SO32-),正确的离子浓度大小为:c(H+)>2c(SO32-)>c(OH-),故D错误;
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理、电荷守恒、物料守恒的含义为解答关键,注意掌握判断离子浓度大小常用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
20.下列反应属于氧化还原反应的是( )
| A. | 二氧化碳和澄清石灰水反应 | B. | 实验室用双氧水制取氧气 | ||
| C. | 碳酸氢钠受热分解 | D. | 氧化铜和稀硫酸反应 |
18.下列实验装置正确且能达到实验目的是( )
| A. | 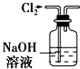 用如图所示装置除去Cl2中含有的少量HCl | |
| B. | 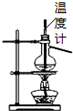 如图所示为石油分馏 | |
| C. | 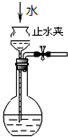 如图所示为检查装置气密性 | |
| D. | 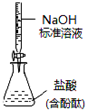 如图所示为测定未知盐酸的浓度 |
15.NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1 mol Na2O2中含有的阴离子数为2 NA | |
| B. | 由H2O2制得2.24 L O2,转移的电子数目为0.4 NA | |
| C. | 常温常压下,8 g O2与O3的混合气体中含有4 NA个电子 | |
| D. | 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02 NA |
2.化学与生活密切相关,能使我们的生活更加美好,下列说法正确的是( )
| A. | 食用蛋白质可以为人体提供氨基酸 | |
| B. | 加碘盐中的碘是I2 | |
| C. | 袋装食品里放置的小袋硅胶是抗氧化剂 | |
| D. | 发酵粉中的小苏打是Na2CO3 |
19.下列有关卤族元素及其化合物的表示正确的是( )
| A. | 氟离子的结构示意图: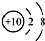 | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | 溴化铵的电子式: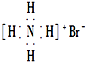 | |
| D. | 质子数为53,中子数为78的碘原子:53131 I |
8.氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注.
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照下表所示的方案完成实验.
(1)实验①和②的目的是探究浓度对反应速率的影响.
同学们进行实验时没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进方法是向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中)(填一种即可).
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图甲所示.
分析该图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
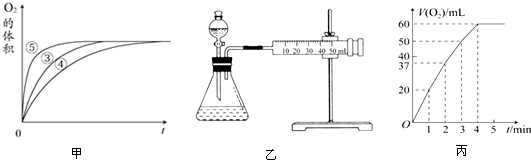
Ⅱ.资料显示,某些金属离子对H2O2的分解起催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图乙所示的实验装置进行实验.
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量单位时间生成O2的体积或生成单位体积O2所需要的时间来比较;
(2)0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示.解释反应速率变化的原因:随着反应的进行,浓度减小,反应速率减慢,计算H2O2的初始物质的量浓度为0.11mol/L.(保留两位有效数字,在标准状况下测定)
(3)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是C(填序号).
A.化学反应速率理论可以指导怎样在一定时间内快出产品
B.勒夏特列原理可以指导怎样使有限原料多出产品
C.催化剂的使用是提高产品产率的有效办法
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照下表所示的方案完成实验.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5%H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5%H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
同学们进行实验时没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进方法是向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中)(填一种即可).
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图甲所示.
分析该图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.

Ⅱ.资料显示,某些金属离子对H2O2的分解起催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图乙所示的实验装置进行实验.
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量单位时间生成O2的体积或生成单位体积O2所需要的时间来比较;
(2)0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示.解释反应速率变化的原因:随着反应的进行,浓度减小,反应速率减慢,计算H2O2的初始物质的量浓度为0.11mol/L.(保留两位有效数字,在标准状况下测定)
(3)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是C(填序号).
A.化学反应速率理论可以指导怎样在一定时间内快出产品
B.勒夏特列原理可以指导怎样使有限原料多出产品
C.催化剂的使用是提高产品产率的有效办法
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
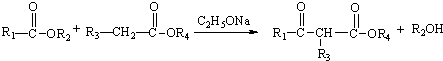
 .
.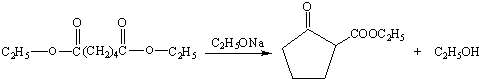 .
.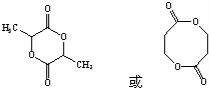 .
.