题目内容
16.用来表示可逆反应2A(g)+B(g)?2C(g)(正反应为放热反应),如图表示的图象中正确的为( )| A. | 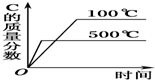 | B. | 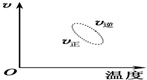 | ||
| C. |  | D. |  |
分析 题中涉及温度、压强的影响,对于反应2A(g)+B(g)?2C(g)(正反应为放热反应),反应物气体的计量数之和大于生成物,增大压强,平衡正向移动,正反应放热,升高温度,平衡逆向移动,以此解答该题.
解答 解:A.温度升高,反应向逆反应方向移动,C的质量分数减小,与图象符合,故A正确;
B.升高温度,正逆反应速率都增大,与图象不符,故B错误;
C.反应物气体的计量数之和大于生成物,增大压强,平衡正向移动,正反应速率大于逆反应速率,故C正确;
D.增大压强,平衡正向移动,A的转化率增大,升高温度,平衡逆向移动,A的转化率减小,图象不符,故D错误.
故选AC.
点评 本题考查化学平衡移动的图象问题,题目难度中等,解答该题的关键是把握图象中曲线的变化特点,结合外界条件对化学平衡的影响分析,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.FeCl3是常见的水处理剂,实验室用铁屑制备无水FeCl3,制备步骤如下:
Ⅰ.称取一定量的铁屑于锥形瓶中,加入过量的6mol•L-1的盐酸,在通风橱中充分反应;
Ⅱ.根据FeCl2的理论产量,加入足量的氧化剂X;
Ⅲ.FeCl3溶液通过一系列操作制得无水FeCl3.
已知:不同温度下六水合FeCl3在水中的溶解度如下:
请回答:
(1)请选择本实验中合适的氧化剂XCD.
A.KMnO4(H+) B.稀硝酸 C.H2O2 D.Cl2
(2)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:
①加入盐酸后,②蒸发浓缩、冷却结晶,③过滤、洗涤,④干燥.
(3)过滤后用少量乙醇洗涤FeCl3•6H2O晶体,选用乙醇的原因是洗去晶体表面的水,减少氯化铁晶体的溶解损耗.
(4)FeCl3的质量分数通常可用碘量法测定:
称取m g无水FeCl3样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-).
①配制FeCl3溶液所需的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需100mL容量瓶;
②在FeCl3质量分数测定的实验过程中,下列说法正确的是CD.
A.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
B.若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中FeCl3的质量分数的测量结果偏高
C.滴定时,左手轻轻向内扣住活塞,手心空握以免碰到活塞使其松动漏出溶液
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③滴定终点的现象是:溶液由蓝色变无色,且半分钟内不变色,样品中FeCl3的质量分数$\frac{162.5cV}{m}%$.
Ⅰ.称取一定量的铁屑于锥形瓶中,加入过量的6mol•L-1的盐酸,在通风橱中充分反应;
Ⅱ.根据FeCl2的理论产量,加入足量的氧化剂X;
Ⅲ.FeCl3溶液通过一系列操作制得无水FeCl3.
已知:不同温度下六水合FeCl3在水中的溶解度如下:
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
(1)请选择本实验中合适的氧化剂XCD.
A.KMnO4(H+) B.稀硝酸 C.H2O2 D.Cl2
(2)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:
①加入盐酸后,②蒸发浓缩、冷却结晶,③过滤、洗涤,④干燥.
(3)过滤后用少量乙醇洗涤FeCl3•6H2O晶体,选用乙醇的原因是洗去晶体表面的水,减少氯化铁晶体的溶解损耗.
(4)FeCl3的质量分数通常可用碘量法测定:
称取m g无水FeCl3样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-).
①配制FeCl3溶液所需的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需100mL容量瓶;
②在FeCl3质量分数测定的实验过程中,下列说法正确的是CD.
A.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
B.若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中FeCl3的质量分数的测量结果偏高
C.滴定时,左手轻轻向内扣住活塞,手心空握以免碰到活塞使其松动漏出溶液
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③滴定终点的现象是:溶液由蓝色变无色,且半分钟内不变色,样品中FeCl3的质量分数$\frac{162.5cV}{m}%$.
4.(1)实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色、易水解,100℃左右时升华,如图是两个学生设计的实验装置、左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示.
已知:4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑
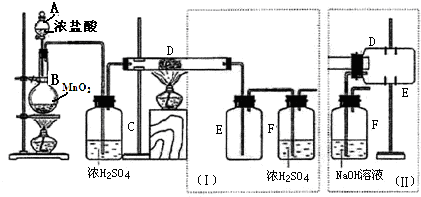
①D中的反应开始前,需排除装置中的空气,应采取的方法是:B中反应进行一段时间后,看到黄绿色气体充满装置B中,再加热装置D的反应管.
②产品收集采用装置(Ⅱ)的主要优点是:导管易被产品堵塞,尾气排入空气,易造成环境污染.
(2)三价铁盐溶液因Fe3+水解而显棕黄色,请以Fe(NO3)3溶液为例,设计实验探究影响盐类水解程度的因素.
①写出Fe(NO3)3水解的离子方程式Fe3++3H2O?Fe(OH)3+3H+.
②参照示例完成下表实验方案的设计.
限选材料:0.5mol•L-1Fe(NO3)3、3.0mol•L-1HNO3、1.0mol•L-1NaOH、NaHCO3固体、蒸馏水、冰水混合物;广泛pH试纸、pH计及其他常见仪器.
已知:4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑

①D中的反应开始前,需排除装置中的空气,应采取的方法是:B中反应进行一段时间后,看到黄绿色气体充满装置B中,再加热装置D的反应管.
②产品收集采用装置(Ⅱ)的主要优点是:导管易被产品堵塞,尾气排入空气,易造成环境污染.
(2)三价铁盐溶液因Fe3+水解而显棕黄色,请以Fe(NO3)3溶液为例,设计实验探究影响盐类水解程度的因素.
①写出Fe(NO3)3水解的离子方程式Fe3++3H2O?Fe(OH)3+3H+.
②参照示例完成下表实验方案的设计.
限选材料:0.5mol•L-1Fe(NO3)3、3.0mol•L-1HNO3、1.0mol•L-1NaOH、NaHCO3固体、蒸馏水、冰水混合物;广泛pH试纸、pH计及其他常见仪器.
| 可能影响因素 | 实验操作 | 预期现象和结论 |
| ①溶液的酸性 | 取少量0.5mol•L-1Fe(NO3)3于试管中,加入几滴3.0mol•L-1HNO3. | 现象:棕黄色溶液颜色变浅; 结论:酸性增强抑制Fe3+水解. |
| ②溶液的浓度 | 取10mL0.5mol•L-1 Fe(NO3)3于烧杯中,用pH计测得pH1.另取90mL蒸馏水加入烧杯,充分搅拌,再测得pH2. | 现象:pH2-pH1<1(或正确表达) 结论:稀释促进水解(或平衡右移) |
| ③溶液的温度 | 取少量0.5mol•L-1Fe(NO3)3于试管中,用酒精灯加热一段时间,观察溶液颜色 | 现象:加热后溶液颜色变深 结论:升高温度促进Fe3+水解 |
11.下列说法中不正确的是( )
| A. | 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应 | |
| B. | 1 mol A(强酸)与1 mol B(强碱)发生中和反应所放出的热量叫做中和热 | |
| C. | 二次电池充电时将电能转化为化学能 | |
| D. | 需要加热才能发生的反应可能是吸热反应也可能是放热反应 |
1.下列描述中正确的是( )
| A. | 已知:P4(白磷,s)═4P(红磷,s)△H<0,则白磷比红磷稳定 | |
| B. | 由CH3CH2CH2CH3(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(g)△H=-2658 kJ•mol-1可知正丁烷的标准燃烧热为2658 kJ•mol-1 | |
| C. | OH-(aq)+H+(aq)═H2O(l)△H=-57.3 kJ•mol-1,故1 mol醋酸与1 mol NaOH完全反应,放出的热量为57.3 kJ•mol-1 | |
| D. | 已知:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1 N2(g)+O2(g)═2NO(g)△H=+180 kJ•mol-1 则2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=-746 kJ•mol-1 |
8.在容积相同的两个密闭容器M和N中,保持温度为150℃,向M容器中加入a mol HI,同时向N容器中加入b mol HI (a>b).当反应2HI(g)?H2 (g)+I2 (g) 达到平衡后,下列说法正确的是( )
| A. | 从反应开始到达到平衡,所需时间tM>tN | |
| B. | 平衡时cM(I2)=c N(I2) | |
| C. | 平衡时I2 蒸气在混合气体中的体积分数:M>N | |
| D. | HI的平衡分解率αM=αN |
5.已知H-H 键的键能为436kJ•mol-1,Cl-Cl键的键能为243kJ•mol-1,H-Cl键的键能为431kJ•mol-1,则H2 (g )+Cl2(g )═2HCl(g ) 的反应热(△H )等于( )
| A. | -183 kJ•mol-1 | B. | +183 kJ•mol-1 | C. | -862 kJ•mol-1 | D. | +862 kJ•mol-1 |
6.下列说法中正确的是( )
| A. | 氢氧化钠的摩尔质量是40g | |
| B. | 1mol氢氧根离子的质量是17g | |
| C. | 1mol氮的质量是14g/mol | |
| D. | 氩气的摩尔质量就是它的相对原子质量 |