题目内容
下列变化需要加入氧化剂才能实现的是( )
| A、S2-→HS- |
| B、Na2SO3→SO2 |
| C、H2S→S |
| D、SO2→S |
考点:氧化还原反应
专题:氧化还原反应专题
分析:需要加入氧化剂才能实现,说明该物质作还原剂,在反应中失电子化合价升高,据此分析解答.
解答:
解:A.S2-→HS-中硫元素化合价不变,则不发生氧化还原反应,故A错误;
B.Na2SO3→SO2中S、O元素化合价都不变,则不发生氧化还原反应,故B错误;
C.H2S→S中S元素化合价由-2价变为0价,失电子化合价升高而作还原剂,故C正确;
D.SO2→S中S元素化合价由+4价变为0价,S元素得电子化合价降低而作氧化剂,故D错误;
故选C.
B.Na2SO3→SO2中S、O元素化合价都不变,则不发生氧化还原反应,故B错误;
C.H2S→S中S元素化合价由-2价变为0价,失电子化合价升高而作还原剂,故C正确;
D.SO2→S中S元素化合价由+4价变为0价,S元素得电子化合价降低而作氧化剂,故D错误;
故选C.
点评:本题以氧化还原反应为载体考查了氧化剂、还原剂,根据元素化合价是否变化及化合价升高还是降低来判断氧化剂、还原剂,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学方程式改写成离子方程式不正确的是( )
| A、CuCl2+2NaOH=Cu(OH)2↓+2NaCl Cu2++2OH-=Cu(OH)2↓ |
| B、BaCO3+2HCl=BaCl2+CO2↑+H2O CO32-+2H+=CO2↑+H2O |
| C、Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3 Ca2++CO32-=CaCO3↓ |
| D、2KOH+H2SO4=K2SO4+2H2O H++OH-=H2O |
下列反应不属于取代反应的是( )
A、CH2═CH2+H2
| |||
B、 +HNO3 +HNO3
| |||
C、CH3CH2OH+CH3COOH
| |||
D、CH4+Cl2
|
科学家已经探明月球上有大量3He存在,以下关于3He的说法不正确的是( )
| A、向两个相同的密闭容器中充入3He和O2,当它们的温度和密度都相同时,两种气体产生的压强不相等 | ||||
| B、3He的质量数为3,所以3He原子的近似相对原子质量为3 | ||||
C、
| ||||
| D、体积相同、密度相同的3He与HD具有相同的中子数 |
下列各离子或分子组能在水溶液中大量共存的是( )
| A、NH4+、H+、NO3-、Fe2+ |
| B、Fe3+、ClO-、Na+、AlO2- |
| C、CO32-、SO32-、Na+、Ba2+ |
| D、SO42-、Cl-、Na+、Al3+ |
 高温下,超氧化钾晶体(KO2)呈立方体结构.如图为超氧化钾晶体的一个晶胞.下列说法正确的是( )
高温下,超氧化钾晶体(KO2)呈立方体结构.如图为超氧化钾晶体的一个晶胞.下列说法正确的是( )| A、KO2中既存在离子键,又存在共价键 | ||
B、每个晶胞含有1个K+和1个O
| ||
C、晶体中与每个K+距离最近的O
| ||
| D、晶体中,所有原子之间都是以离子键结合 |
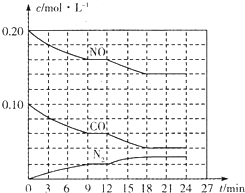 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.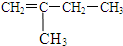 和Br2发生加成反应时,产物的结构简式为
和Br2发生加成反应时,产物的结构简式为