题目内容
2.工业上,采用电解法处理NO制备NH4NO3变废为宝.工作原理如图所示:图中阳极反应式为NO-3e-+2H2O=NO3-+4H+,通入的X物质的化学式是NH3,若电源提供15mol电子,理论上最多制备NH4NO3的物质的量为5mol.
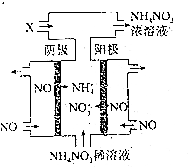
分析 工业上电解NO制备NH4NO3,阳极发生氧化反应,NO被氧化生成NO3-,阴极发生还原反应,NO被还原生成NH4+,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,据此解答.
解答 解:工业上电解NO制备NH4NO3,阳极发生氧化反应,NO被氧化生成NO3-,阴极发生还原反应,NO被还原生成NH4+,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,通入的X物质的化学式是NH3,
电解生成硝酸铵与硝酸,而硝酸与氨气转化为硝酸铵,电源提供15mol电子,生成NO3-为$\frac{15mol}{3}$=5mol,由硝酸根守恒,理论上最多制备NH4NO3的物质的量为5mol,
故答案为:NO-3e-+2H2O=NO3-+4H+;NH3;5mol.
点评 本题考查电解原理,侧重于考查学生的综合运用能力,计算制备硝酸铵物质的量为易错点,难度中等,注意基础知识的积累掌握.

练习册系列答案
相关题目
12.下列试剂不能把等物质的量浓度的Na2CO3溶液、NaHCO3溶液鉴别开的是( )
| A. | CaCl2溶液 | B. | 澄清石灰水 | C. | 稀盐酸 | D. | 酚酞溶液 |
13.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
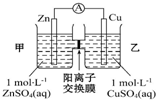

| A. | 铜电极上发生反应Cu-2e-=Cu2+ | |
| B. | 电池工作一段时间后,乙池的c(SO42- )减小 | |
| C. | 电子从锌极经过导线移向铜极 | |
| D. | 电池工作一段时间后,甲池的c(Zn2+ )增加 |
17.在密闭容器中,对于可逆反应A+3B?2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )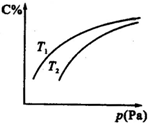

| A. | B一定为气体 | |
| B. | A一定为气体 | |
| C. | 若正反应方向△H<0,则T1>T2 | |
| D. | 压强增大时,混合气体的平均相对分子质量减小 |
7.对气体反应:mA+nB?eC,温度(T)、压强(P)、时间(t)与生成物的体积百分数C%的关系图,下列结论正确的是( )
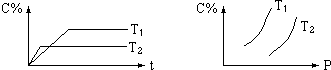
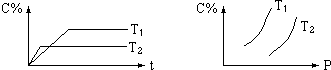
| A. | T1<T2 | B. | m+n<e | ||
| C. | 正反应是吸热反应 | D. | 逆反应是放热反应 |
14.有八种物质:①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯⑧环己烯,既能使KMnO4酸性溶液褪色,又能与溴水反应使之褪色的是( )
| A. | ①④⑤⑧ | B. | ②④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |