题目内容
16.将9.6g纯铜片投入足量的某硝酸溶液中,铜片完全溶解.放出气体由导管过盛有蒸馏水的洗气瓶充分反应,测得洗气瓶中液体增重Vg.排水后理论上从洗气瓶出气口收集到气体(S.T.P)的体积为( )| A. | 2.24升 | B. | 3.36升 | C. | 4.48升 | D. | 5.6升 |
分析 Cu与硝酸反应生成硝酸铜、N的氧化物和水,气体由导管过盛有蒸馏水的洗气瓶充分反应后最终收集气体为NO,整个过程中Cu失去电子数等于N得到电子数,以此来解答.
解答 解:整个过程中Cu失去电子数等于N得到电子数,由电子守恒可知,n(NO)=$\frac{\frac{9.6g}{64g/mol}×(2-0)}{(5-2)}$=0.1mol,理论上从洗气瓶出气口收集到气体(S.T.P)的体积为0.1mol×22.4L/mol=2.24L,
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化、电子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
7.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-═Mg2+ | |
| B. | 负极可能会发生副反应Mg+2H2O═Mg(OH)2+H2↑ | |
| C. | 电池放电时Cl-由负极向正极迁移 | |
| D. | 正极反应式为AgCl+e-═Ag+Cl- |
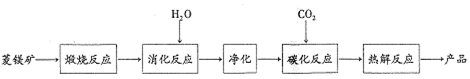
11.水合碱式碳酸镁[4MgCO3•Mg(OH)2•4H2O〕,又称轻质碳酸镁.常利用菱镁矿(质量含量为碳酸镁90%,碳酸钙10%〕碳化法制取:
(1)根据下列表格数据,选择消化反应的最佳温度70℃;理由是温度进一步升高同等幅度,转化率几乎不变,但能耗增加.
(2)碳化反应可生成Mg(HCO3)2,生成Mg(HCO3)2的化学方程式为Mg(OH)2+2CO2═Mg(HCO3)2.
(3)流程图中煅烧反应和热解反应可以为碳化反应提供二氧化碳源.
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5时,可以认为完全除去.常温时当调节溶液pH为9.5时,此时Mn2+小于10-5mol/L,不会沉淀出来.
②如果把Fe2+转化为Fe3+,从环境角度选择最合适的氧化剂为C.
A.Ca(C1O)2 B.Cl2 C.H2O2 D.HNO3
③下列方案中,较好的为方案2,理由是加入碳酸钠的产品中易混入更多杂质,不易提纯.


(1)根据下列表格数据,选择消化反应的最佳温度70℃;理由是温度进一步升高同等幅度,转化率几乎不变,但能耗增加.
| 消化温度/℃ | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 转化率/% | 50.3 | 58.2 | 85.1 | 85.2 | 90.7 | 91.2 | 91.5 |
(3)流程图中煅烧反应和热解反应可以为碳化反应提供二氧化碳源.
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5时,可以认为完全除去.常温时当调节溶液pH为9.5时,此时Mn2+小于10-5mol/L,不会沉淀出来.
| 物质 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| Ksp | 10-11 | 10-39 | 10-17 | 10-14 |
A.Ca(C1O)2 B.Cl2 C.H2O2 D.HNO3
③下列方案中,较好的为方案2,理由是加入碳酸钠的产品中易混入更多杂质,不易提纯.

1.常温常压下,点燃100mlH2S和O2的混合气体,充分反应恢复到原状况,气体的体积变为58ml,这58ml气体的成分是( )
| A. | H2S | B. | SO2 | C. | SO2、O2 | D. | SO2、H2S |
5.某有机物的结构如图,关于该有机物的说法不正确的是( )
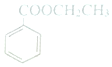

| A. | 分子式为C9H10O2 | |
| B. | 能发生取代、加成反应 | |
| C. | 苯环上的一氯代物有3种 | |
| D. | 在酸性条件下水解产物均能与NaOH溶液反应 |
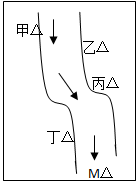 在一条鱼虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示,箭头表示河水流向),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色混浊,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.
在一条鱼虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示,箭头表示河水流向),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色混浊,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.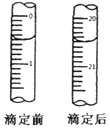 检测血液中的Ca2+能够帮助判断多种疾病.某研究小组测定血液样品中Ca2+的含量(l00mL血液中含Ca2+的质量),实验步骤如下:
检测血液中的Ca2+能够帮助判断多种疾病.某研究小组测定血液样品中Ca2+的含量(l00mL血液中含Ca2+的质量),实验步骤如下: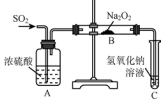 (1)已知Na2O2能与CO2反应,可用来呼吸面具中的做生氧剂.该反应:
(1)已知Na2O2能与CO2反应,可用来呼吸面具中的做生氧剂.该反应:
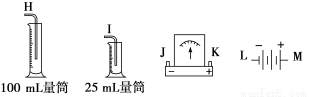
 现象是_________________
现象是_________________