题目内容
1-20号元素中最外层电子数是次外层电子数三倍的原子是( )
| A、氧原子 | B、硫原子 |
| C、锂原子 | D、硼原子 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:根据原子核外电子排布规则,最外层最多不超过8个电子,最外层电子数是次外层电子数三倍,则说明次外层只能有2个电子,因此该元素含有的电子数为2+6=8.
解答:
解:根据原子核外电子排布规则,最外层最多不超过8个电子,
最外层电子数是次外层电子数三倍,则说明次外层只能有2个电子,
因此该元素含有的电子数为2+6=8,质子数=核外电子数=8,为氧原子,
故选:A.
最外层电子数是次外层电子数三倍,则说明次外层只能有2个电子,
因此该元素含有的电子数为2+6=8,质子数=核外电子数=8,为氧原子,
故选:A.
点评:本题考查原子核外电子排布知识,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
某原子的基态电子排布为1s22s22p63s23p63d64s2,该元素不可能的价态是( )
| A、-1 | B、+2 | C、+3 | D、0 |
下列实验方案合理的是( )

| A、配制银氨溶液:质量分数为2% 氨水中加入过量的硝酸银溶液 |
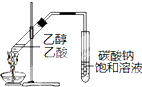
| B、制备乙酸乙酯:用如右图所示的实验装置 |
| C、鉴定溴乙烷中的溴原子:向溴乙烷中加入硝酸酸化的硝酸银溶液 |
| D、鉴别地沟油和矿物油:加入足量氢氧化钠溶液加热 |
基态铬原子的电子排布式是( )
| A、1S22S22p63S23p64S14p5 |
| B、1S22S22p63S23p63d6 |
| C、1S22S22p63S23p64S23d4 |
| D、1S22S22p63S23P63d54S1 |
设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温下,50g SO2和CO2的混合气体中可能含有2NA个氧原子 |
| B、1mol Cl2与足量的铁反应,转移的电子数为3NA |
| C、1L0.1mol?L-1氨水含有0.1lNA个OH- |
| D、1mol甲醇中含有C-H键的数目为3NA |
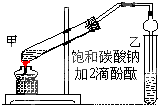 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下: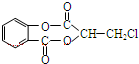 )在一定条件下可以发生如图所示的转化(其他产物和水已略去).
)在一定条件下可以发生如图所示的转化(其他产物和水已略去).