题目内容
正确掌握化学用语是学好化学的基础.下列化学用语中不正确的是( )
| A、乙烯的结构简式CH2=CH2 |
B、CH4分子的球棍模型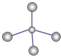 |
C、Ca2+的结构示意图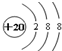 |
| D、乙醇的分子式 C2H6O |
考点:结构简式,原子结构示意图,球棍模型与比例模型
专题:化学用语专题
分析:A.乙烯含有碳碳双键;
B.CH4分子为正四面体结构,碳原子半径比氢原子大;
C.Ca2+的质子数为20,电子数为18;
D.乙醇的分子式为:C2H6O.
B.CH4分子为正四面体结构,碳原子半径比氢原子大;
C.Ca2+的质子数为20,电子数为18;
D.乙醇的分子式为:C2H6O.
解答:
解:A.乙烯含有碳碳双键,结构简式为:CH2=CH2,故A正确;
B.CH4分子为正四面体结构,碳原子半径比氢原子大,应为: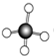 故B错误;
故B错误;
C.Ca2+的质子数为20,电子数为18,故结构示意图为: ,故C正确;
,故C正确;
D.乙醇的分子式为:C2H6O,故D正确;
故选B.
B.CH4分子为正四面体结构,碳原子半径比氢原子大,应为:
 故B错误;
故B错误; C.Ca2+的质子数为20,电子数为18,故结构示意图为:
 ,故C正确;
,故C正确;D.乙醇的分子式为:C2H6O,故D正确;
故选B.
点评:本题考查结构简式、离子结构示意图、球棍模型、分子式等化学用语,为高频考点,题目难度不大.把握化学用语的规范应用是解答的关键.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
下列有关化学用语正确的是( )
| A、次氯酸的结构式:H-Cl-O |
B、二氧化碳的比例模型: |
C、甲基的电子式: |
| D、纤维素的通式:(C6H12O6)n |
X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知( )
| A、X的原子半径大于Y的原子半径 |
| B、X的电负性小于Y的电负性 |
| C、X的氧化性大于Y的氧化性 |
| D、X的第一电离能小于Y的第一电离能 |
硫酸镁和硫酸铝溶液等体积混合后,Al3+浓度为0.1mol?L-1,SO42-浓度为0.3mol?L-1,则混合液中镁离了的浓度为( )
| A、0.45mol?L-1 |
| B、0.3mol?L-1 |
| C、0.15mol?L-1 |
| D、0.1mol?L-1 |
关于下列各装置图的叙述中,不正确的是( )
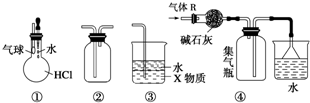

| A、装置①可验证HCl气体在水中的溶解性 |
| B、装置②可用于收集H2、NH3、Cl2、HCl、NO2、NO等 |
| C、装置③中X为四氯化碳,可用于吸收氨气或氯化氢 |
| D、装置④可用于干燥、收集氨气,并吸收多余的氨气 |
下列实验操作中,正确的是( )
| A、蒸发溶液时,边加热加搅拌,直至蒸发皿内的液体蒸干 |
| B、量取25.00LKMnO4溶液时,应选择酸式滴定管 |
| C、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4注入容量瓶中加水稀释,边注入边搅拌 |
| D、配制一定物质的量浓度的溶液时,若未洗涤烧杯和玻璃棒,则会导致所配溶液的物质的量浓度偏高 |
下列化学用语正确的是( )
A、
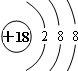 | ||||
B、HCl的电子式 | ||||
C、质量数为37的氯原子
| ||||
D、CH4分子的比例模型 |
能正确表示下列反应的离子方程式的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、电解饱和食盐水:2Cl-+H2O═2OH-+H2↑+Cl2↑ |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
化学与人类生产、生活、社会可持续发展密切相关.下列有关说法正确的是( )
| A、高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2═2O3有单质参加,属于氧化还原反应 |
| B、人造纤维,合成纤维和光导纤维都是有机高分子化合物 |
| C、大量燃烧化石燃料排放的废气中含大量CO2、SO2造成大气污染,从而使雨水pH=5.6形成酸雨 |
| D、加热能杀死流感病毒是因为病毒的蛋白质受热变性 |