题目内容
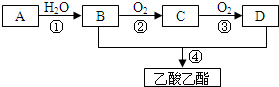
 观察下列结构简式,回答下列问题:
观察下列结构简式,回答下列问题:I.乙酸的结构简式为

(1)a的名称是
(2)c的名称是
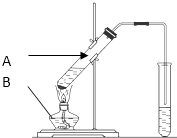
Ⅱ.乙酸乙酯的制备
(1)反应装置中用到的仪器:A、
(2)乙醇与乙酸制乙酸乙酯的化学方程式
(3)实验中浓硫酸作用
(4)饱和Na2CO3溶液的作用是
考点:乙酸的化学性质,乙酸乙酯的制取
专题:实验题,有机化学基础
分析:Ⅰ.根据结构式写出乙酸的组成基团;
Ⅱ.(1)根据装置图指出所用仪器;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应,该反应为可逆反应;
(3)浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(4)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层.
Ⅱ.(1)根据装置图指出所用仪器;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应,该反应为可逆反应;
(3)浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(4)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层.
解答:
解:I.从乙酸的结构简式可知,乙酸由-CH3、-CO-、-OH组成,名称分别为甲基、羰基和羟基,故答案为:甲基;羟基;
II.(1)从装置图可知,A为试管,B为酒精灯,故答案为:试管;酒精灯;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,反应为CH3COOH+C2H5OH
CH3COOC2H5+H2O,该反应为可逆反应,故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O;
(3)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化剂,吸水剂,故答案为:催化作用、吸水作用;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,故答案为:吸收乙酸,溶解乙醇,冷凝乙酸乙酯蒸气且减小乙酸乙酯在水中的溶解度,以利于分层析出.
II.(1)从装置图可知,A为试管,B为酒精灯,故答案为:试管;酒精灯;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,反应为CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
(3)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化剂,吸水剂,故答案为:催化作用、吸水作用;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,故答案为:吸收乙酸,溶解乙醇,冷凝乙酸乙酯蒸气且减小乙酸乙酯在水中的溶解度,以利于分层析出.
点评:本题考查乙酸的性质和乙酸乙酯的制备,解答时须注意酯化反应的原理和饱和碳酸钠溶液的作用,题目难度不大.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
| A、硝酸为弱电解质 |
| B、该溶液1 mL稀释至100 mL后,pH小于3 |
| C、向该溶液中加入等体积、等浓度的氢氧化钡溶液,混合后溶液pH=7 |
| D、该溶液中水电离出的c(H+)=1×10-13 mol/L |
反应A(g)+3B(g)?2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )
| A、v (C)=30 mol/(L?min) |
| B、v (D)=0.4 mol/(L?s) |
| C、v (B)=0.6 mol/(L?s) |
| D、v (A)=12 mol/(L?min) |
某酸性溶液中存在较多的Fe3+,则溶液中还可能大量存在的离子组是( )
| A、OH-、Cl-、Na+ |
| B、SO42-、Cl-、NH4+ |
| C、ClO-、HCO3-、K+ |
| D、I一、Fe2+、Ba2+ |