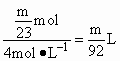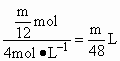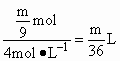题目内容
Na、Mg、Al分别与盐酸反应.
(1)若盐酸足量,等物质的量的Na、Mg、Al产生的氢气质量之比为________.
(2)若盐酸足量,等质量的Na、Mg、Al产生H2的质量之比为________,溶液增重质量之比为________.
(3)若盐酸等质量且足量,充分反应后所得溶液质量相等,则Na、Mg、Al质量之比为________.
(4)若盐酸浓度相等,体积相等,投入的Na、Mg、Al质量相等,反应后有一种金属剩余,该金属是________.
(5)称取Na、Mg、Al各m g,在室温下分别与V L 4 mol·L-1的盐酸充分反应,试推断,在下列三种情况下,V的取值范围(用含m的表达式表示).
①Al与盐酸反应放出H2最多时,________.
②Na与盐酸反应放出H2最多时,________.
③Mg和Al与盐酸反应产生H2一样多时,________.
解析:
|
答案:(1)1∶2∶3 (2) (3) (4)Al (5)①V> 解析:(1)盐酸足量,有下列关系: 2Na+2HCl 1 mol Mg+2HCl 1 mol 1 mol 2Al+6HCl 1 mol 2Na+2HCl V(HCl)= Mg+2HCl V(HCl)= 2Al+6HCl V(HCl)= ①保证等质量的Na、Mg、Al与盐酸反应,Al产生的H2最多,即Na、Mg完全反应,HCl仍有剩余,即V(HCl)> ②保证等质量的Na、Mg、Al与盐酸反应,Na产生H2最多,即Na过量,HCl不足,过量Na与水反应,而Mg、Al不与水反应,即V(HCl)< ③等质量的Na、Mg、Al与盐酸反应,Mg、Al产生H2一样多,即Mg、Al与盐酸反应时,HCl都不足或Mg恰好反应完全,过量Na与水反应,而Mg、Al不与水反应,即V(HCl)≤ |