题目内容
6.已知:RCHO+CH2(COOH)2$\stackrel{一定条件}{→}$RCH=C(COOH)2+H2O
RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑
A与芳香族化合物B在一定条件下反生成C,进一步反应生成抗氧化剂阿魏酸(见图)
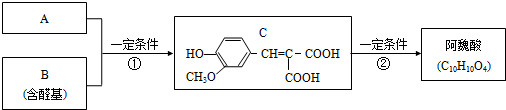
A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体.
(1)A的结构简式是CH2(COOH)2.
(2)在中学学过知识里 B不可能发生的反应是e (填序号)
a、取代反应 b、加成反应c、氧化反应d、还原反应e、水解反应 f、显色反应
(3)等物质的量C分别与足量的Na、浓溴水、NaOH、NaHCO3反应时消耗Na、Br2、NaOH、NaHCO3的物质的量之比是3:2:3:2
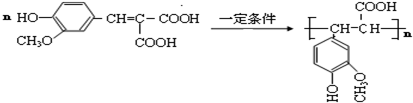
(4)写出利用阿魏酸在一定条件下生成抗氧化性的高分子化合物的方程式:
 .
.(5)写出符合下列条件的阿魏酸所有的同分异构体的结构简式:
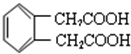 .
.①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种;
③1mol该同分异构体与足量NaHCO3反应生成2mol CO2气体;
④该同分异构体进行核磁共振氢谱分析发现只有4种峰.
分析 由反应信息RCHO+CH2(COOH)2$\stackrel{一定条件}{→}$RCH=C(COOH)2+H2O可知,形成C的物质分别为CH2(COOH)2、 ,A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体,B含有醛基,所以A为CH2(COOH)2,B为
,A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体,B含有醛基,所以A为CH2(COOH)2,B为 ,C的分子式为C11H10O6,阿魏酸的分子式为C10H10O4,分子组成减少1个CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,阿魏酸的结构简式为
,C的分子式为C11H10O6,阿魏酸的分子式为C10H10O4,分子组成减少1个CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,阿魏酸的结构简式为 ,据此解答.
,据此解答.
解答 解:由反应信息RCHO+CH2(COOH)2$\stackrel{一定条件}{→}$RCH=C(COOH)2+H2O可知,形成C的物质分别为CH2(COOH)2、 ,A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体,B含有醛基,所以A为CH2(COOH)2,B为
,A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体,B含有醛基,所以A为CH2(COOH)2,B为 ,C的分子式为C11H10O6,阿魏酸的分子式为C10H10O4,分子组成减少1个CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,阿魏酸的结构简式为
,C的分子式为C11H10O6,阿魏酸的分子式为C10H10O4,分子组成减少1个CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,阿魏酸的结构简式为 ,
,
(1)通过以上分析知,A结构简式为CH2(COOH)2,故答案为:CH2(COOH)2;
(2)B是 ,含有酚羟基,可以发生取代反应、氧化反应、酯化反应,能与氯化铁发生显色反应,含有醛基,可以发生氧化反应、还原反应、加成反应,含有苯环可以发生加成反应,不能发生水解反应,故选e;
,含有酚羟基,可以发生取代反应、氧化反应、酯化反应,能与氯化铁发生显色反应,含有醛基,可以发生氧化反应、还原反应、加成反应,含有苯环可以发生加成反应,不能发生水解反应,故选e;
(3)C中含2个-COOH和1个酚-OH,均能与Na、NaOH反应,只有-COOH与NaHCO3反应,只有1个酚-OH的邻位能与溴发生取代反应,且C=C能与溴水发生加成反应,则等物质的量C分别与足量的Na、浓溴水、NaOH、NaHCO3反应时消耗Na、Br2、NaOH、NaHCO3的物质的量之比是3:2:3:2,故答案为:3:2:3:2;
(4)该反应方程式为 ,
,
故答案为: ;
;
(5)阿魏酸的同分异构体符合下列条件:
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种,说明苯环上含有两种氢原子;
③1mol该同分异构体与足量NaHCO3反应生成2mol CO2气体,说明含有两个羧基;
④该同分异构体进行核磁共振氢谱分析发现只有4种峰,说明含有四种氢原子;
符合条件的同分异构体结构简式为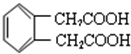 ,故答案为:
,故答案为: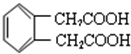 .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析判断及获取信息利用信息解答问题能力,明确官能团及其性质关系结合题给信息解答问题是解本题关键,难点是同分异构体结构简式的确定.

| A. | CuO | B. | FeC13 | C. | CuS | D. | FeS |
①CH4、C2H6 ②C3H6、C3H8 ③C2H4、C3H8O ④C2H4、C3H6.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ④ |
| A. | 燃煤时加入适量石灰石,可减少废气中SO2的含量 | |
| B. | 京津冀、长三角、珠三角雾霾的形成与煤的燃烧、化工厂大量排放含硫、含氮氧化物、颗粒物和汽车排放的尾气等有关 | |
| C. | pH小于7.0的降雨通常称为酸雨 | |
| D. | 使用洁净能源、为汽车安装尾气转化装置、对硝酸厂排放的废气进行碱处理能有效控制氮氧化物对空气的污染 |
| A. | 小于0.9mol | B. | 等于0.9mol | ||
| C. | 在0.45mol与0.9mol之间 | D. | 大于0.9mol |
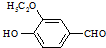 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.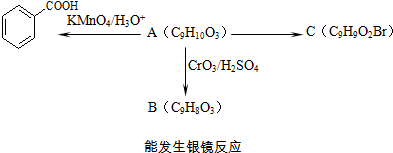
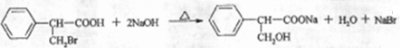
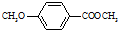 )是一种医药中间体.
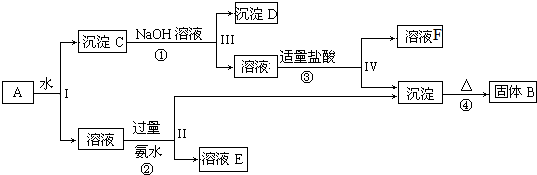
)是一种医药中间体. )合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭头下方,试剂或原料写在箭头上方,中间产物填在图中的方框内.
)合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭头下方,试剂或原料写在箭头上方,中间产物填在图中的方框内.

 .
. 2NH3
2NH3