题目内容
由硅、铁、铝组成的试样19.4g均匀地分成等质量的两份:一份跟足量稀硫酸反应可产生气体a L;一份与足量的氢氧化钠溶液反应也能产生同种气体b L,合并两次所收集的气体共11.2L,试分析此试样的组成?(气体均在标准状况下测得其体积,且a=b)
考点:有关混合物反应的计算
专题:计算题
分析:硅、铝与氢氧化钠反应生成氢气,铁不与氢氧化钠反应.铁、铝与稀硫酸反应生成氢气,硅不与硫酸反应,两过程生成的氢气相等,且依据体积可以计算物质的量,反应中Al都表现+3价,铁表现+2价、硅表现+4价,列式计算即可.
解答:
解:设硅、铁、铝的质量分别为:2x、2y和2z,生成氢气的物质的量为:
=0.5mol,依据题意有:
,解得2x=2.8g,2y=11.2g,2z=5.4g,答:硅、铝、铁分别为2.8g、11.2g、5.4g.
| 11.2L |
| 22.4L/mol |
|
|
点评:本题考查混合物的有关计算,难度较大,清楚发生的反应,设出未知数,利用氢气体积以及所给质量关系列出方程是解决本题的关键.

练习册系列答案
相关题目
右图为元素周期表短周期的一部分.关A~F六种元素的叙述正确的是( )
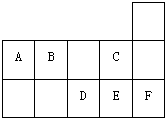

| A、A、B、D、E四种元素所形成的最高价含氧酸中D酸性最强 |
| B、形成的简单阴离子半径:C>B>D>E |
| C、D、E、F形成的单质都是双原子分子 |
| D、A与E形成的分子是一种常见有机溶剂 |
根据碘与氢气反应的热化学方程式(碘为气态或固态),下列判断正确的是( )
(ⅰ) I2(?)+H2(g)?2HI(g)+9.48kJ (ⅱ) I2(?)+H2(g)?2HI(g)-26.48kJ.
(ⅰ) I2(?)+H2(g)?2HI(g)+9.48kJ (ⅱ) I2(?)+H2(g)?2HI(g)-26.48kJ.
| A、ⅰ中碘为气态,ⅱ中碘为固态 |
| B、反应(ⅰ)的产物比反应(ⅱ)的产物稳定 |
| C、1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ |
| D、1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
从海带灰中可以提取碘,主要反应为:Cl2+2I-═I2+2Cl-,下列说法不正确的是( )
| A、该反应属于置换反应 |
| B、反应中I-离子发生还原反应 |
| C、Cl2的氧化性比I2的氧化性强 |
| D、生成1mol I2转移2mol e- |
下列说法不正确的是( )
| A、126C、136C、146C 为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以126C 的核素形式存在.146C为放射性核素,可用于同位素示踪 |
| B、汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
| C、道尔顿、汤姆生、卢瑟福、玻尔等科学家的研究不断更新人们对原子结构的认识 |
| D、地沟油由于混有一些对人体有害的杂质而不能食用,可加工制成生物柴油,生物柴油的成分与从石油中提取的柴油成分不同 |
下列反应既属于化合反应,又属于氧化还原反应的是( )
A、CO+CuO
| ||||
| B、2FeCl2+Cl2=2FeCl3 | ||||
| C、CaO+H2O=Ca(OH)2 | ||||
| D、2Al+3CuSO4=3Cu+2Al2(SO4)3 |

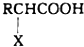 +HX
+HX