题目内容
X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置如下表.已知X元素最低负化合价的绝对值与其原子最外层电子数相等,Y是地壳中含量最多的金属元素.下列说法错误的是( )
| X | ||
| Z |
| A、X位于第二周期第ⅣA族 |
| B、原子半径由小到大的顺序为:W<Z<Y |
| C、Z、W两元素的气态氢化物中,Z的气态氢化物更稳定 |
| D、无论氧气是否过量,Z在氧气中燃烧的产物唯一 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X元素最低负化合价的绝对值与其原子最外层电子数相等,则X为ⅣA族元素;
Y是地壳中含量最多的金属元素,则Y为Al元素,又X、Y、Z、W是原子序数依次增大的短周期主族元素,X的原子序数小于13,则X只能为C元素;
X为C元素,则Z一定位于周期表中第三周期ⅥA族,即Z为S元素,W的原子序数大于S,且为主族元素,则W只能为Cl元素,
根据以上分析可知:X为C元素、Y为,Al元素、Z为S元素、W为Cl元素,
据此对各选项进行判断.
Y是地壳中含量最多的金属元素,则Y为Al元素,又X、Y、Z、W是原子序数依次增大的短周期主族元素,X的原子序数小于13,则X只能为C元素;
X为C元素,则Z一定位于周期表中第三周期ⅥA族,即Z为S元素,W的原子序数大于S,且为主族元素,则W只能为Cl元素,
根据以上分析可知:X为C元素、Y为,Al元素、Z为S元素、W为Cl元素,
据此对各选项进行判断.
解答:
解:X为主族元素,X元素最低负化合价的绝对值与其原子最外层电子数相等,则X为ⅣA族元素;
Y是地壳中含量最多的金属元素,则Y为Al元素,又X、Y、Z、W是原子序数依次增大的短周期主族元素,则X只能为C元素;
X为C元素,则Z一定位于周期表中第三周期ⅥA族,即Z为S元素,W的原子序数大于S,且为主族元素,则W只能为Cl元素,
根据以上分析可知:X为C元素、Y为Al元素、Z为S元素、W为Cl元素,
A.X为C元素,位于周期表中第二周期第ⅣA族,故A正确;
B.Y为Al元素、Z为S元素、W只能为Cl元素,电子层越多,原子半径越多,若电子层相同,核电荷数越大,半径越小,所以三种原子的半径从小到大的顺序为:W<Z<Y,故B正确;
C.Z为S元素、W为Cl元素,非金属性越强,其气态氢化物的稳定性越强,非金属性Z<W,则W的气态氢化物稳定,故C错误;
D.Z为S元素,硫单质在空气燃烧生成二氧化硫,与氧气的量无关,故D正确;
故选C.
Y是地壳中含量最多的金属元素,则Y为Al元素,又X、Y、Z、W是原子序数依次增大的短周期主族元素,则X只能为C元素;
X为C元素,则Z一定位于周期表中第三周期ⅥA族,即Z为S元素,W的原子序数大于S,且为主族元素,则W只能为Cl元素,
根据以上分析可知:X为C元素、Y为Al元素、Z为S元素、W为Cl元素,
A.X为C元素,位于周期表中第二周期第ⅣA族,故A正确;
B.Y为Al元素、Z为S元素、W只能为Cl元素,电子层越多,原子半径越多,若电子层相同,核电荷数越大,半径越小,所以三种原子的半径从小到大的顺序为:W<Z<Y,故B正确;
C.Z为S元素、W为Cl元素,非金属性越强,其气态氢化物的稳定性越强,非金属性Z<W,则W的气态氢化物稳定,故C错误;
D.Z为S元素,硫单质在空气燃烧生成二氧化硫,与氧气的量无关,故D正确;
故选C.
点评:本题考查了元素位置结构性质的相互关系应用,题目难度中等,注意掌握原子结构与元素周期表、元素周期律之间的关系,正确推断各元素名称为解答关键,试题侧重基础知识考查,有利于培养学生灵活应用所学知识解决实际问题的能力.

练习册系列答案
相关题目
现有甲、乙、丙、丁四种常温下呈气态的化合物,都是由两种相同的短周期元素组成,它们的分子中所含电子数如下表所示下列关于四种物质的推断中正确的是( )
| 分子代号 | 甲 | 乙 | 丙 | 丁 |
| 电子数 | 10 | 14 | 16 | 18 |
| A、四种气体中至少有两种气体分子互为同分异构体 |
| B、四种气体通入溴的四氯化碳溶液中,都能使其褪色 |
| C、气体丙的所有原子在同一平面上 |
| D、鉴别乙和丙两种气体,可以用酸性高锰酸钾溶液 |
化学科学需要借助化学专用语言来描述,下列化学用语的书写正确的是( )
A、CO2分子的比例模型示意图: | ||
B、质量数为40的钙原子:
| ||
C、Ca2+的结构示意图为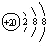 | ||
D、水合钠离子示意图: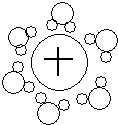 |
下列各组中的离子,能在水溶液中大量共存的是( )
| A、K+、H+、SO42-、OH- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、Na+、Cu2+、SO42-、Cl- |
下列物质:①盐酸 ②食盐水 ③熔化的氯化钠 ④液态氯化氢 ⑤铜 ⑥氨水 ⑦SO3 ⑧醋酸,其中可以导电并且属于强电解质的是( )
| A、只有③ | B、①②③⑥⑧ |
| C、④⑤ | D、全部都是 |
在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡的标志是( )
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、容器内B、C、D的浓度之比为2:1:1 |
| D、混合气体的总物质的量 |