题目内容
3.下列实验方法能够达到要求的是( )| A. | 把铁片与电源正极相连、碳棒与电源负极相连放入食盐水中,证明铁被保护 | |
| B. | 电解AlCl3溶液制取铝单质 | |
| C. | 用25 mL滴定管量出14.80 mL溶液 | |
| D. | 用pH试纸测得某碱溶液的pH为12.6 |
分析 A.铁片与电源正极相连,为阳极,失去电子;
B.电解AlCl3溶液,生成氢氧化铝、氢气、氯气;
C.滴定管的感量为0.01mL;
D.pH试纸测定值为正整数.
解答 解:A.铁片与电源正极相连,为阳极,失去电子,加快铁的腐蚀,故A错误;
B.电解AlCl3溶液,生成氢氧化铝、氢气、氯气,应电解熔融氧化铝冶炼Al,故B错误;
C.滴定管的感量为0.01mL,则用25 mL滴定管量出14.80 mL溶液,故C正确;
D.pH试纸测定值为正整数,则用pH试纸测得某碱溶液的pH为12或13,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握原电池、电解、仪器的使用、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
14.下列说法不正确的是( )
| A. | CO2、SiO2的晶体结构类型不同 | |
| B. | 加热硅、硫晶体使之熔化,克服的作用力不同 | |
| C. | HF比HCl稳定是因为HF间存在氢键 | |
| D. | NaOH、NH4Cl晶体中既有离子键又有共价键 |
15.二氧化硫是硫的重要化合物,在生产、生活中有广泛应用.二氧化硫有毒,并且是形成酸雨的主要气体.无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要.完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通.
石灰-石膏法和碱法是常用的烟气脱硫法.
石灰-石膏法的吸收反应为:SO2+Ca(OH)2═CaSO3↓+H2O.吸收产物亚硫酸钙由管道输送至氧化塔氧化,
反应为2CaSO3+O2+4H2O=2CaSO4•2H2O.其流程如图: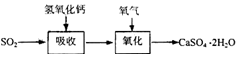
碱法的吸收反应为SO2+2NaOH=Na2SO3+H2O.碱法的特点是氢氧化钠碱性强、吸收快、效率高.
其流程如图: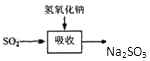
已知:
(1)石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是利用SO2是酸性氧化物,可与碱反应.和碱法相比,石灰-石膏法的优点是原料易得,吸收成本低.
(2)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示).
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通.
石灰-石膏法和碱法是常用的烟气脱硫法.
石灰-石膏法的吸收反应为:SO2+Ca(OH)2═CaSO3↓+H2O.吸收产物亚硫酸钙由管道输送至氧化塔氧化,
反应为2CaSO3+O2+4H2O=2CaSO4•2H2O.其流程如图:

碱法的吸收反应为SO2+2NaOH=Na2SO3+H2O.碱法的特点是氢氧化钠碱性强、吸收快、效率高.
其流程如图:

已知:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
(2)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示).
11.高温、催化剂条件下,某反应达到平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| A. | 该反应的焓变为负值 | |
| B. | 升高温度,正反应速率增大,逆反应速率减小,平衡正向移动 | |
| C. | 2CO2(g)+2H2(g)?2CO(g)+2H2O(g) 的平衡常数K1=K2 | |
| D. | 若恒容、恒温下充入CO,则K值变大 |
18.下列各组物质中,满足表中图示物质在一定条件下能一步转化的组合只有( )
| 序号 | X | Y | Z | W | 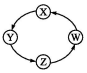 |
| ① | Cu | CuSO4 | Cu(OH)2 | CuO | |
| ② | Na | NaOH | Na2CO3 | NaCl | |
| ③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
| ④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
| A. | ①②③ | B. | ①③④ | C. | ②④ | D. | ①④ |
8.下列说法中正确的是( )
| A. | 羧酸的官能团是羟基 | |
| B. | 羟基和氢氧根中含有的电子数不同 | |
| C. | 在氧气中燃烧只生成二氧化碳和水的有机物一定是烃 | |
| D. | 乙醇与钠反应生成氢气,此现象说明乙醇具有酸性 |
12. 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:
(1)等物质的量浓度的 a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为cbda(填字母).
(2)常温下,0.1mol•L-1的CH3COOH 溶液加水稀释,下列表达式的数据变大的是B.
A.C(H+) B.C(H+)/C(CH3COOH) C.C(H+)•C(OH-)
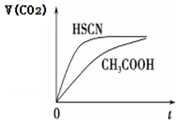
(3)25℃时,将 20mL 0.1mol•L-1 CH3COOH 溶液和 20mL0.1mol•L-1HSCN溶液分别与20mL 0.1mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快; 反应结束后所得两溶液中,(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
(4)25℃时,在 CH3COOH 与 CH3COONa 的混合溶液中,若测得 pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值),c(CH3COO-)/c(CH3COOH)=17.
(5)用离子方程式表示Na2CO3溶液呈碱性的原因CO32-+H2O?HCO3-+OH-.
 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.7×10-5 | 6.2×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
(2)常温下,0.1mol•L-1的CH3COOH 溶液加水稀释,下列表达式的数据变大的是B.
A.C(H+) B.C(H+)/C(CH3COOH) C.C(H+)•C(OH-)
(3)25℃时,将 20mL 0.1mol•L-1 CH3COOH 溶液和 20mL0.1mol•L-1HSCN溶液分别与20mL 0.1mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快; 反应结束后所得两溶液中,(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
(4)25℃时,在 CH3COOH 与 CH3COONa 的混合溶液中,若测得 pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值),c(CH3COO-)/c(CH3COOH)=17.
(5)用离子方程式表示Na2CO3溶液呈碱性的原因CO32-+H2O?HCO3-+OH-.
13.下列气体通入水中所得溶液呈碱性的是( )
| A. | CO2 | B. | SO2 | C. | NH3 | D. | HC1 |