题目内容
14.X、Y、Z、R、W是原子序数依次增大的短周期主族元素,X是元素周期表中原子半径最小的元素.X与Z同主族,Y与W同主族,R最外层电子数是电子层数的2倍.下列叙述正确的是( )| A. | 原子半径:W>R>Z | |
| B. | W的最高价氧化物对应的水化物酸性比R的强 | |
| C. | W与X形成的是离子化合物 | |
| D. | W的气态氢化物的热稳定性比Y的强 |
分析 X、Y、Z、R、W是原子序数依次增大的短周期主族元素,Y与W同主族,则Y处于第二周期,W处于第三周期,X是周期表中原子半径最小的元素,则X为H元素,X与Z同主族,Z的原子序数大于Y,则Z为Na;R处于第三周期,R最外层电子数是电子层数的2倍,则R为S元素;W原子序数最大,故W为Cl,则Y为F元素,结合元素周期律解答.
解答 解:X、Y、Z、R、W是原子序数依次增大的短周期主族元素,Y与W同主族,则Y处于第二周期,W处于第三周期,X是周期表中原子半径最小的元素,则X为H元素,X与Z同主族,Z的原子序数大于Y,则Z为Na;R处于第三周期,R最外层电子数是电子层数的2倍,则R为S元素;W原子序数最大,故W为Cl,则Y为F元素.
A.同周期从左向右原子半径在减小,则原子半径为Z(Na)>R(S)>W(Cl),故A错误;
B.非金属性W(Cl)>R(S),故W的最高价氧化物对应的水化物酸性比R的强,故B正确;
C.W与X形成物质为HCl,属于共价化合物,故C错误;
D.非金属性W(Cl)<Y(F),非金属性越强,氢化物的稳定性越强,W的气态氢化物的热稳定性比Y的若,故D错误,
故选B.
点评 本题考查结构性质位置关系应用,难度不大,注意对元素周期律的理解掌握.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
9.除去混在碳酸钠粉末中的少量碳酸氢钠,最合理的方法是( )
| A. | 加热 | B. | 加入氢氧化钠溶液 | ||
| C. | 加入盐酸 | D. | 加入CaCl2溶液 |
2. 恒容密闭容器中发生反应:2X(g)?Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图.下列叙述正确的是( )
恒容密闭容器中发生反应:2X(g)?Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图.下列叙述正确的是( )
 恒容密闭容器中发生反应:2X(g)?Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图.下列叙述正确的是( )
恒容密闭容器中发生反应:2X(g)?Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图.下列叙述正确的是( )| A. | M点的正反应速率v正大于N点的逆反应速率v逆 | |
| B. | T2下,在0~t1时间内v(Y)=$\frac{(a-b)}{t_1}$(mol•L-1•min-1) | |
| C. | 该反应进行到M点放出的热量大于进行到W点放出的热量 | |
| D. | M点时再加入一定量X,平衡后X的转化率减小 |
9.某溶液中存在大量的OH-、Na+、SO42-,该溶液中还可能大量存在的离子是( )
| A. | Al3+ | B. | Ba2+ | C. | NH4+ | D. | CO32ˉ |
19.下列有机物的命名正确的是( )
| A. | 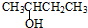 2-羟基丁烷 2-羟基丁烷 | B. |  :3-乙基-1-丁烯 :3-乙基-1-丁烯 | ||
| C. |  :1,3-二溴丙烷 :1,3-二溴丙烷 | D. | 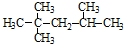 :2,2,3-三甲基戊烷 :2,2,3-三甲基戊烷 |
6.下列关于氮的固定的说法错误的是( )
| A. | 氮的固定包括人工固氮和自然固氮 | B. | 工业合成氨属于人工固氮 | ||
| C. | 自然固氮中氮元素被氧化 | D. | 氮的固定中参与元素至少有两种 |
3.中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是( )
| A. |  火法炼铜 | B. |  粘土制陶瓷 | C. |  树皮造纸 | D. |  打磨磁石制 |
