题目内容
19.由A、B、C、D四种金属按表中装置进行实验.| 装置 | 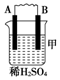 |  |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)装置丙中溶液的pH变大(填“变大”、“变小”或“不变”).
分析 甲装置中,二价金属A不断溶解说明该装置构成了原电池,且A失电子发生氧化反应而作负极,B作正极;乙中C的质量增加,说明C上铜离子得电子发生还原反应,则C作原电池正极,B作负极;丙装置中A上有气体产生,说明A上氢离子得电子发生还原反应,则A作原电池正极,D作负极,据此分析解答.
解答 解:(1)该装置中,二价金属A不断溶解说明A失电子发生氧化反应生成金属阳离子进入溶液而作负极,所以负极电极反应式为A-2e-═A2+,故答案为:A-2e-═A2+;
(2)乙装置中,C的质量增加说明C电极上铜离子得电子发生还原反应,则C作正极,电极反应式为Cu2++2e-═Cu,故答案为:Cu2++2e-═Cu;
(3)丙装置中A上有气体产生,说明A上氢离子得电子发生还原反应而作正极,D作负极,正极上氢离子逐渐析出而导致氢离子浓度逐渐减小,则溶液的pH逐渐变大,故答案为:变大.
点评 本题考查了原电池原理,根据原电池电极上得失电子来判断正负极,一般来说,作原电池负极的金属金属活动性顺序强,难度不大.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案
相关题目
9.纯锌和稀硫酸反应速率很小,为了加快锌的溶解和放出H2的速率,可以加入少量( )
| A. | 硫酸铜晶体 | B. | 稀盐酸 | C. | 镁带 | D. | 碘化钾溶液 |
10.下列装置所示的实验中,能达到实验目的是( )
| A. |  分离碘酒中的碘和酒精 | B. |  实验室制氨气 | ||
| C. | 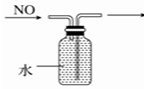 排水集气法收集NO | D. |  除去Cl2中的HCl |
7.具备基本的化学实验技能是进行科学探究的基础和保证.下列有关实验操作正确的 是( )
| A. |  点燃酒精灯 | B. | 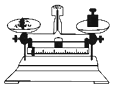 称量固体 | C. |  液体加热 | D. |  量取9.0mL液体 |
14.已知反应
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
由此可以推断下列结论正确的是( )
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
由此可以推断下列结论正确的是( )
| A. | 1 mol碳完全燃烧放出的热大于110.5 kJ | |
| B. | ①的焓变为221 kJ•mol-1 | |
| C. | 浓硫酸与稀NaOH溶液完全反应生成1 mol水时放热为57.3 kJ | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
8.实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种.下列根据实验事实得出的结论错误的是( )
| A. | 取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有 Na2CO3 | |
| B. | 取一定量固体,溶解,向溶液中加人适量CaO粉末,充分反应后观察到有白色沉淀生成,说明 原固体中一定含有Na2CO3 | |
| C. | 取一定量固体,溶解,向溶液中滴加适量AgNO3溶液后有白色沉淀生成,这个现象不能说明原固体中一定含有NaCl | |
| D. | 称取3.80g固体,加热至恒重,质量减少了 0.620g.用足童稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3 |