题目内容
下列物质燃烧热相同的是( )
| A、1mol C2H40.5mol C4H8 |
| B、2mol正丁烷 2mol异丁烷 |
| C、1mol 金刚石 12g石墨 |
| D、3mol乙醇 2mo乙醇 |
考点:燃烧热
专题:化学反应中的能量变化
分析:燃烧热是指1 mol物质完全燃烧生成稳定氧化物时所放出的热量.一般元素对应的稳定氧化物分别为C→CO2,H→H2O(l),S→SO2.燃烧热是物质的性质,与量的多少无关.
解答:
解:燃烧热是指1 mol物质完全燃烧生成稳定氧化物时所放出的热量.一般元素对应的稳定氧化物分别为C→CO2,H→H2O(l),S→SO2.燃烧热是物质的性质,与量的多少无关.
A、1molC2H4和0.5mol C4H8物质不同,燃烧热不同,故A错误;
B、2mol正丁烷和2mol异丁烷物质不同,燃烧热不同,故B错误;
C、1mol 金刚石和12g石墨物质不同,燃烧热不同,故C错误;
D、3mol乙醇和2mo乙醇是同种物质,燃烧热相同,和量的多少无关,故D正确.
故选:D.
A、1molC2H4和0.5mol C4H8物质不同,燃烧热不同,故A错误;
B、2mol正丁烷和2mol异丁烷物质不同,燃烧热不同,故B错误;
C、1mol 金刚石和12g石墨物质不同,燃烧热不同,故C错误;
D、3mol乙醇和2mo乙醇是同种物质,燃烧热相同,和量的多少无关,故D正确.
故选:D.
点评:考查燃烧热的概念,难度较小,注意把握燃烧热的含义可燃物为1mol,一般C→CO2,H→H2O(l),S→SO2.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A、标准状况下,22.4LCO2含有的分子数为0.1NA |
| B、等物质的量的N2和CO所含分子数均为NA |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、3.8gNH4中含有的H原子数为0.2NA |
卤素单质从F2到I2在常温常压下的聚集状态由气态、液态到固态的原因是( )
| A、原子间的化学键键能逐渐减小 |
| B、范德华力逐渐增大 |
| C、原子半径逐渐增大 |
| D、氧化性逐渐减弱 |
下列事实不能用平衡移动原理解释的是( )
| A、实验室中常用排饱和食盐水的方法收集氯气 |
| B、配制FeC13溶液时加入少量的盐酸 |
| C、实验室利用双氧水制备氧气时使用催化剂 |
| D、工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
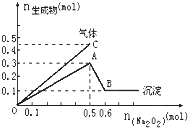 向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )| A、1:1:2 |
| B、2:2:1 |
| C、1:2:2 |
| D、9:2:4 |
已知某气态烃1mol最多可与2molHCl发生加成反应,所得产物与Cl2发生取代反应时,若将氢原子全部取代,需要8mol Cl2,则该烃可能是( )
| A、丙炔 | B、乙炔 |
| C、2-丁炔 | D、2-丁烯 |