题目内容
两种元素原子X和Y,Y原子的第三层比氩原子的第三层少6个电子,Y原子的第二层电子数恰为X原子第二层电子数的2倍,则X、Y的质子数分别为( )
| A、14和12 | B、6和12 |
| C、12和6 | D、8和12 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:原子的质子数等于原子核外电子总数,根据原子核外电子的排布规律:先排第一层,最多容纳2个电子,再排第二层,最多容纳8个电子,再排第三层,最多容纳18个电子,最外层不超过8个电子.
解答:
解:Y原子的第三层比氩原子的第三层少6个电子,Y是Mg;Y原子的第二层电子数恰为X原子第二层电子数的2倍,所以X的第二层为4个电子,没有第三层,即第三层电子数是0,故X为C,则X、Y的质子数分别为6和12,
故选B.
故选B.
点评:本题考查原子核外电子排布,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
在密闭容器中充入4molSO2和3molO2,一定条件下平衡:2SO2(g)+O2(g)?2SO3(g)△H=-a kJ/mol,反应中测得SO2的转化率为90%,则在此条件下反应放出的热量( )
| A、1.8a kJ |
| B、a kJ |
| C、2a kJ |
| D、0.9a kJ |
在体积一定的密闭容器中加入一定量的物质A、B、C,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)?xC(g),符合如图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强).在图中,Y轴是指( )
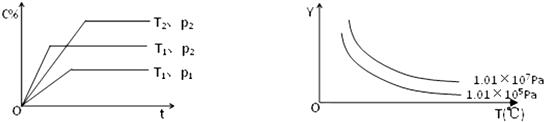

| A、反应物A的百分含量 |
| B、反应体系内分子的总数目 |
| C、平衡混合气体的密度 |
| D、平衡混合气体的平均摩尔质量 |
在一定温度下,固定容积中发生可逆反应:N2(g)+3H2(g)?2NH3(g),下列情况一定能说明此反应达到平衡状态的是( )
| A、体系的压强或混合气体密度不再改变 |
| B、各物质的浓度保持不变 |
| C、反应速率υ(N2):υ(H2):υ(NH3)=1:3:2 |
| D、单位时间内消耗0.1molN2,同时消耗0.3mol H2 |
在2NO2?N2O4的可逆反应中,下列状态属于平衡状态的是( )
| A、υ正=υ逆≠0时的状态 |
| B、NO2全部转变成N2O4的状态 |
| C、c(NO2)=c(N2O4)的状态 |
| D、N2O4不再分解的状态 |
下列状态的物质,既能导电又属于电解质的是( )
| A、KCl溶液 |
| B、液态HCl |
| C、熔融的NaOH |
| D、蔗糖溶液 |
设NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A、2.7g金属铝与足量盐酸反应失去的电子数为0.3NA | ||
| B、常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA | ||
| C、0.5mol/L Fe2(SO4)3溶液中,SO42-的数目为1.5NA | ||
D、C2H4和C3H6的混合物ag,所含原子总数为
|
由下列反应:Cu+2FeCl3→2FeCl2+CuCl2,CuCl2+Fe→FeCl2+Cu,确定Fe2+、Fe3+、Cu2+的氧化性强弱顺序为( )
| A、Fe2+>Cu2+>Fe3+ |
| B、Fe3+>Cu2+>Fe2+ |
| C、Fe3+>Fe2+>Cu2+ |
| D、Fe2+>Fe3+>Cu2+ |