题目内容
16.甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中均含18个电子,甲是气态氢化物,在水中分步电离出两种阴离子,下列推断错误的是( )| A. | 若某钠盐溶液含甲电离出的阴离子,则该溶液既可能与酸反应又可能与碱反应 | |
| B. | 若乙与氧气的摩尔质量相同,则乙只能由2种元素组成 | |
| C. | 若丙中含有第2周期ⅣA族的元素,则丙可能是甲烷的同系物 | |
| D. | 若丁中各元素质量比跟甲中各元素质量比相同,则丁中一定含有-1价的元素 |
分析 甲是18电子的气态氢化物,在水中分步电离出两种阴离子,则其水溶液为二元弱酸,甲为H2S.
A.如为NaHS,则与酸、碱都反应;
B.乙与氧气的摩尔质量相同,可能为CH3 OH、N2H4等;
C.丙中含有二周期IVA族的元素,可能为CH3OH等;
D.丁和甲中各元素质量比相同,丁应为H2O2.
解答 解:A.甲是18电子的氢化物,且其水溶液为二元弱酸,不难得出甲为H2S,若盐溶液为Na2S溶液,溶液呈碱性,不能与碱反应,若为NaHS,其溶液呈酸性,既能与盐酸等反应生成H2S,也能与Na0H反应生成Na2S,故A正确;
B.氧气的摩尔质量为32g/mol,乙的摩尔质量也为32g/mol,且含有18电子,CH3OH符合,由3种元素组成,故B错误;
C.丙中含有第二周期IVA族元素为C,如C2H6符合,C2H6是CH4的同系物,故C正确;
D.H2S中元素的质量比为1:16,H2O2分子中元素的质量比也为1:16,则丁为H2O2,H2O2中氧元素的价态为-1价,故D正确.
故选B.
点评 本题考查原子结构与元素周期率知识,为高频考点,侧重于学生的分析能力的考查,题目难度较大,注意常见18电子物质的种类以及性质,解答本题时注意能找出反例.

练习册系列答案
相关题目
7.下列有关物质应用的说法正确的是( )
| A. | 小苏打是面包发酵粉的主要成分之一 | |
| B. | 盐类都可用作调味品 | |
| C. | 铝罐可久盛食醋 | |
| D. | 生石灰用作食品抗氧化剂 |
8.在1L 1mol/L的氨水中,下列说法正确的是( )
| A. | 含1 mol NH3分子 | B. | 含NH3和NH4+之和为1mol | ||
| C. | 含NH3、NH4+、NH3•H2O之和为1 mol | D. | 含NH3•H2O 1mol |
12.四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法正确的是( )
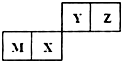

| A. | M与Z形成的化合物中只存在离子键 | |
| B. | X的最简单气态氢化物的热稳定性比Z的强 | |
| C. | 原子半径Z>Y | |
| D. | M的最高价氧化物对应水化物能与NaOH溶液反应 |
6.对烷烃CH3CH(C2H5)CH(C2H5)CH(CH3)2的命名,正确的是( )
| A. | 2,3-二甲基-4-乙基戊烷 | B. | 2-甲基3,4-二乙基戊烷 | ||
| C. | 2,4-二甲基-3-乙基己烷 | D. | 2,5-二甲基-3-乙基己烷 |
3.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数递增的同周期元素,且最外层电子数之和为 15,Y与Z可形成YZ2分子,Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X>M | |
| B. | XZ2、X2M2、W2Z2均为共价化合物 | |
| C. | 由Z、M两种元素形成化合物的分子式一定为M2Z | |
| D. | 由 Y、Z、M 三种元素形成的化合物可以既有离子键,又有共价键 |
4.下列说法不正确的是( )
| A. | SiO2不与任何酸反应 | |
| B. | Cl2是一种有强烈刺激性气味的有毒气体 | |
| C. | NO2易溶于水,且能与水反应 | |
| D. | SO2是酸性氧化物,是形成酸雨的主要气体 |
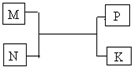 A、B、C、D、E、F是短周期元素,周期表中A与B、B与C相邻;C与E同主族;A与C最外层电子数之比为2:3,B的最外层电子数比C的最外层电子数少1个; F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞溶液变红.
A、B、C、D、E、F是短周期元素,周期表中A与B、B与C相邻;C与E同主族;A与C最外层电子数之比为2:3,B的最外层电子数比C的最外层电子数少1个; F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞溶液变红.