题目内容
下列说法中错误的是( )
| A、NaHCO3溶液中碳元素主要以HCO3-存在 |
| B、Na2CO3溶液中滴加酚酞呈红色,加热红色变深 |
| C、NH4Cl溶液呈酸性这一事实能说明一水合氨为弱碱 |
| D、在稀醋酸中加醋酸钠固体能促进醋酸的电离 |
考点:钠的重要化合物,弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:基本概念与基本理论
分析:A、碳酸氢钠是碳酸氢根离子和钠离子构成分析;
B、碳酸钠溶液中碳酸根离子水解显碱性,水解是吸热过程,加热促进水解;
C、氯化铵水解显酸性说明铵根离子是弱碱阳离子;
D、醋酸溶液中存在电离平衡,加入醋酸钠,增大醋酸根离子浓度,平衡左移;
B、碳酸钠溶液中碳酸根离子水解显碱性,水解是吸热过程,加热促进水解;
C、氯化铵水解显酸性说明铵根离子是弱碱阳离子;
D、醋酸溶液中存在电离平衡,加入醋酸钠,增大醋酸根离子浓度,平衡左移;
解答:
解:A、碳酸氢钠是碳酸氢根离子和钠离子构成,NaHCO3溶液中碳元素主要以HCO3-存在,故A正确;
B、碳酸钠溶液中碳酸根离子水解显碱性,水解是吸热过程,加热促进水解减小增强,Na2CO3溶液中滴加酚酞呈红色,加热红色变深,故B正确;
C、氯化铵水解显酸性说明铵根离子是弱碱阳离子,推断对应一水合氨为弱碱,故C正确;
D、醋酸溶液中存在电离平衡,加入醋酸钠,增大醋酸根离子浓度,平衡左移,抑制醋酸电离,故D错误;
故选D.
B、碳酸钠溶液中碳酸根离子水解显碱性,水解是吸热过程,加热促进水解减小增强,Na2CO3溶液中滴加酚酞呈红色,加热红色变深,故B正确;
C、氯化铵水解显酸性说明铵根离子是弱碱阳离子,推断对应一水合氨为弱碱,故C正确;
D、醋酸溶液中存在电离平衡,加入醋酸钠,增大醋酸根离子浓度,平衡左移,抑制醋酸电离,故D错误;
故选D.
点评:本题考查了物质性质分析,盐类水解和弱电解质电离平衡的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
用下列装置不能达到有关实验目的是( )
A、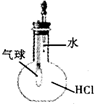 验证HCl的溶解性 |
B、 制备Fe(OH)2 |
C、 干燥并收集NH3 |
D、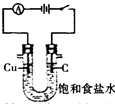 利用电解法制H2和Cl2 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-?H++B2-,则下列说法中一定正确的是( )
| A、NaHB溶液可能存在以下关系:c(Na+)>c(HB-)>c(OH-)>c(H+) |
| B、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
| C、NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) |
| D、在Na2B溶液中一定有:c(OH-)=c(H+)+c(HB-)+2c(H2B) |
下列离子方程式书写正确的是( )
| A、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ |
| B、向NaHCO3溶液中滴加AlCl3溶液:Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
| C、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O |
| D、SO2气体通入Ba(NO3)2溶液中:SO2+H2O+Ba2+═BaSO3↓+2H+ |
下列说法正确的是( )
| A、蛋白质溶液中加入食盐会出现白色沉淀 |
| B、目前世界上最重要的矿物燃料是乙醇 |
| C、葡萄糖在人体内氧化分解属于吸热反应 |
| D、化学反应中的能量变化,只表现为热量的变化 |
在下列各溶液中,离子一定能大量共存的是( )
| A、室温下,pH=13的溶液中:K+、Al3+、Cl-、SO42- |
| B、含有1mol?L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- |
| C、由水电离的c(H+)=10-12 mol?L-1的溶液中,K+、Na+、Cl-、SO4 |
| D、室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
下列化学反应属于吸热反应的是( )
| A、碘的升华 |
| B、生石灰溶于水 |
| C、镁和稀硫酸反应 |
| D、木炭和二氧化碳反应 |
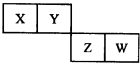 短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是其电子层数的2倍,下列叙述正确的是( )
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是其电子层数的2倍,下列叙述正确的是( )| A、原子半径的大小顺序为:rZ>rW>rX>rY |
| B、元素W的含氧酸的酸性一定比Z的含氧酸的酸性强 |
| C、工业上是通过热还原获得元素W的单质 |
| D、XZ2和XW4中化学键的类型不同 |