题目内容
(1)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?
(2)某有机物的结构简式为HOOC-CH=CHOH.
①请你写出该有机物官能团的名称: 、 、 .
②验证该有机物中含有-COOH官能团常采用的方法是 ,产生的现象为 .
(2)某有机物的结构简式为HOOC-CH=CHOH.
①请你写出该有机物官能团的名称:
②验证该有机物中含有-COOH官能团常采用的方法是
考点:有机物的结构和性质,有机物分子中的官能团及其结构
专题:
分析:(1)根据“冰醋酸(熔点16.6℃)”的特点(在室温较低时,无水乙酸就会凝结成像冰一样的晶体),只要使冰醋酸的温度稍微高于室温,它就会变成液态可以取出;只要把试剂瓶带到高于16.6℃的地方即可,当然方法多种;
(2)①根据有机物的结构特点判断有机物含有的官能团;
②羧基具有酸的通性:使石蕊试液变红、能和碳酸钠反应生成二氧化碳等等.
(2)①根据有机物的结构特点判断有机物含有的官能团;
②羧基具有酸的通性:使石蕊试液变红、能和碳酸钠反应生成二氧化碳等等.
解答:
解:(1)因为冰醋酸的熔点16.6℃,所以可以把试剂瓶带到大于16.6℃的地方或者水浴稍微加热或者用热毛巾捂热等,
故答案为:水浴微热、用热毛巾热敷、将试剂瓶拿到高于16.6℃的房间内等;
(2)①根据有机物的结构简式可知,该有机物含有羟基、羧基、碳碳双键三种官能团,故答案为:羟基;羧基;碳碳双键.
②羧基具有酸的通性,能使石蕊试液变红,能和碳酸钠反应生成二氧化碳等,所以可用碳酸钠溶液或石蕊试液验证.
故答案为:用该物质和碳酸钠溶液反应是否有气泡生成或能否使石蕊试液变红;产生气泡或变红.
故答案为:水浴微热、用热毛巾热敷、将试剂瓶拿到高于16.6℃的房间内等;
(2)①根据有机物的结构简式可知,该有机物含有羟基、羧基、碳碳双键三种官能团,故答案为:羟基;羧基;碳碳双键.
②羧基具有酸的通性,能使石蕊试液变红,能和碳酸钠反应生成二氧化碳等,所以可用碳酸钠溶液或石蕊试液验证.
故答案为:用该物质和碳酸钠溶液反应是否有气泡生成或能否使石蕊试液变红;产生气泡或变红.
点评:本题考查了官能团的判断、物质的性质等知识点,难度不大,结构决定性质,性质体现结构,熟记官能团的性质是解题的关键.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
为确定下列久置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的是( )
| A、Na2SO3溶液(BaCl2) |
| B、FeCl2溶液(KSCN) |
| C、KI(淀粉溶液) |
| D、NaOH溶液(盐酸) |
三氯生是一种抗菌剂,其结构如图所示,遇含氯自来水能生成有毒的三氯甲烷.下列说法不正确的是( ) 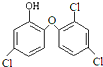

| A、三氯生的分子式是C12H7Cl3O2 |
| B、三氯甲烷与甲烷均无同分异构体 |
| C、1 mol三氯生最多能与6 mol H2反应 |
| D、1 mol三氯生最多能与4mol NaOH反应 |
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A、生成40.0LN2(标准状况) |
| B、有0.250molKNO3被氧化 |
| C、转移电子的物质的量为2.5mol |
| D、被氧化的N原子的物质的量为3.75mol |
已知金属钾有如下性质:①钾的密度比水小;②钾的熔点低;③钾与水反应时放出热量;④钾与水反应后溶液呈碱性.某学生将一小块金属钾投入滴有酚酞溶液的水中,以上实验能证明上述四点性质中的( )
| A、①④ | B、①②④ |
| C、①③④ | D、①②③④ |
下列装置能形成原电池的是( )
A、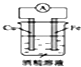 |
B、 |
C、 |
D、 |
设NA为阿伏加德罗常数的值,则下列说法正确的是( )
| A、电解精炼铜时,若阴极得到电子数为2NA,阳极减少64g |
| B、200mL某硫酸强碱盐中含有1.5NA个SO42-离子,同时含有NA个金属阳离子,该盐物质的量浓度是2.5mol/L |
| C、常温常压下78g Na2O2固体中所含阴、阳离子总数为4NA |
| D、一定条件下足量的Fe粉与浓硫酸反应,转移电子数一定为2NA |