题目内容
12.下列物质发生状态变化时,克服了分子间相互作用力的是( )| A. | 食盐熔化 | B. | 晶体硅熔化 | C. | 碘升华 | D. | 氢氧化钠熔化 |
分析 先判断晶体类型和断键方式,再判断克服的作用力,分子间的作用力决定了分子晶体的物理性质,属于分子晶体的三态变化是克服的是分子间的作用力.
解答 解:A.食盐是离子晶体,微粒间的作用力是离子键,故A错误;
B.晶体硅是原子晶体熔化克服的是共价键,故B错误;
C.碘升华是分子晶体克服的是分子间作用力,故C正确;
D.氢氧化钠是离子晶体,熔化发生离子键键的断裂,克服的是离子键,故D错误.
故选C.
点评 本题考查了微粒之间的作用力,难度不大,此类题的解题方法是:先判断断键方式,再判断克服的作用力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.在120℃时,某气态烃和CH4的混合气体10L,在足量90LO2中充分燃烧又恢复到120℃,测得气体体积为100L.则该气态烃可能为( )
| A. | C2H2 | B. | C2H4 | C. | C3H8 | D. | C2H6 |
7.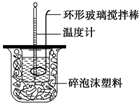 测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )
 测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )| A. | 实验装置中小烧杯杯中低于大烧杯杯口 | |
| B. | 用浓硫酸代替了稀硫酸 | |
| C. | 分多次把NaOH溶液倒入盛有硫酸的小烧杯中 | |
| D. | 用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度 |
17.下列有关化学键的叙述,正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 化学键的常见类型为离子键、共价键和氢键 | |
| D. | 离子化合物中一定含有离子键 |
1.下列化学用语表达正确的是( )
| A. | HF的电子式为: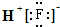 | B. | HClO的结构式:H-Cl-O | ||
| C. | CO2的电子式为: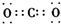 | D. | Cl-的结构示意图: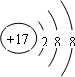 |
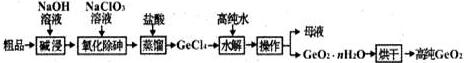
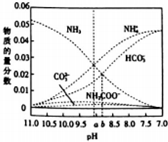 氮及其化合物在生产、生活中有着重要作用.
氮及其化合物在生产、生活中有着重要作用.
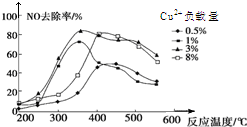 雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应:
雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应: