题目内容
7.下列有关生活生产中的叙述合理的是( )| A. | 水库的钢闸门与电源负极相连以防止其生锈,该法即牺牲阳极的阴极保护法 | |
| B. | 明矾和漂白粉用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| C. | 铜的精炼工业和电镀铜工业,均可采用CuSO4溶液做电解质溶液 | |
| D. | 工业上合成氨采用500℃左右的温度,其原因是适当加快NH3的合成速率,催化剂在500℃左右时其活性最好,且能提高H2的转化率 |
分析 A、与电源负极相连为外接电源的阴极保护法;
B、明矾没有强氧化性不能杀菌消毒;
C、根据铜的精炼和电镀铜的原理分析;
D、催化剂不能使平衡移动.
解答 解:A、水库的钢闸门与电源负极相连以防止其生锈,此时铁作阴极,该法为外接电源的阴极保护法,故A错误;
B、明矾中的铝离子在水中水解生成氢氧化铝胶体能吸附水中的悬浮颗粒,从而起到净水作用,但是明矾没有强氧化性不能杀菌消毒,漂白粉有强氧化性能用于自来水的杀菌消毒,故B错误;
C、铜的精炼中粗铜为阳极,纯铜为阴极,硫酸铜溶液为电解质溶液,电镀铜时待镀金属为阴极,铜为阳极,硫酸铜溶液为电镀液,故C正确;
D、在500℃左右时催化剂的活性最大,所以选择采用500℃左右的温度进行但使用催化剂时平衡不移动,故不能提高氢气的转化率,故D错误.
故选C.
点评 本题考查了金属的电化学腐蚀和防护、明矾净水原理、漂白粉的杀菌消毒原理、电镀和电解精炼,题目涉及的知识点较多,侧重于反应原理的应用的考查,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.今有吸热反应C+CO2?2CO和放热反应N2+3H2?2NH3,两者的反应速率为分别为V1和V2,当温度升高时,V1和V2的变化情况为( )
| A. | 同时增大 | B. | 同时减少 | C. | V1增大,V2减小 | D. | V1减小,V2增大 |
18.化学与我们的生活息息相关,下列有关基本营养物质的说法正确的是( )
| A. | 人体内没有水解纤维素的酶,所以纤维素在人体内没有任何作用 | |
| B. | 变质的油脂有难闻的哈喇味是因为油脂发生了加成反应 | |
| C. | 吃馒头时越嚼越感觉甜是因为淀粉发生了水解反应 | |
| D. | 牛奶中含有丰富的蛋白质,所以羊毛衫上沾有奶渍时可以用加酶洗衣粉洗涤 |
12.A、B、C、D四种短周期元素,0.5molA的元素的离子得到NA个电子后被还原为中性原子;0.4gA的氧化物恰好与100mL0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等.B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素与C元素处于同一主族.下列说法正确的是( )
| A. | A元素位于元素周期表的第三周期ⅢA族 | |
| B. | B的单质只能与硫酸反应,不能与氢氧化钠溶液反应 | |
| C. | C的气态氢化物的沸点比D的气态氢化物的沸点高 | |
| D. | D的非金属性比C的非金属性强 |
19.甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下.下列说法正确的是( )
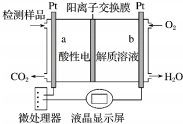

| A. | 溶液中H+从b向a定向移动 | |
| B. | a电极发生的电极反应为CH3OH-6e-+H2O=CO2↑+6H+ | |
| C. | 当电路中有1 mol e-转移时,正极区n(H+)增加1 mol | |
| D. | 将酸性电解质溶液改为碱性电解质溶液,该测试仪不可能产生电流 |
19.下列颜色变化不属于化学变化的是( )
| A. | 向品红溶液中滴加亚硫酸 | |
| B. | KMnO4溶液滴定NaHSO3溶液,溶液由无色变为浅红色30s不褪色,即为滴定终点 | |
| C. | 久置氯水变成无色 | |
| D. | 向苯酚溶液中滴加FeCl3 |
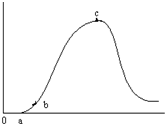 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如右的坐标曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如右的坐标曲线来表示,回答下列问题:
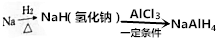 四氢铝钠(NaAlH4)在化工生产中有着重要应用.其简易合成工艺流程如图所示.
四氢铝钠(NaAlH4)在化工生产中有着重要应用.其简易合成工艺流程如图所示.