题目内容
13.工业合成氨的反应是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂.已知形成1 mol H-H键、1 mol N-H键、1mol N≡N键放出的能量分别为436 kJ、391 kJ、946 kJ.则:(1)写出工业合成氨的化学方程式N2(g)+3H2(g)?2NH3(g).
(2)若0.5mol N2完全反应生成NH3可放出(填“吸收”或“放出”)热量46kJ.
(3)如果将0.5mol N2和1.5mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是该反应是可逆反应,反应物不能完全转化为生成物,所以放出的热量要小于46kJ.
(4)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过5min后,数据如下,则用N2表示的化学反应速率为0.4mol/L/min.
| 物质 | N2 | H2 | NH3 |
| 反应前 | 16mol | xmol | 0 |
| 5min | ymol | 28mol | 8mol |
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
f.反应达到最大限度.
分析 (1)根据反应物和生成物书写方程式;
(2)在反应N2+3H2?2NH3中,断裂3molH-H键、1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,该反应热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,根据氮气和焓变关系式计算放出的热量;
(3)该反应是可逆反应,反应物不能完全转化为生成物;
(4)先计算氨气平均反应速率,再根据同一可逆反应中同一条件下不同物质的反应速率之比等于其计量数之比计算氮气平均反应速率;
(5)可逆反应达到平衡状态时,同一物质的正逆反应速率相等且不等于0,反应达到最大限度.
解答 解:(1)该反应方程式为N2(g)+3H2(g)?2NH3(g),故答案为:N2(g)+3H2(g)?2NH3(g);
(2)在反应N2+3H2?2NH3中,断裂3molH-H键、1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,该反应热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,1mol氮气完全反应放出92kJ能量,则0.5mol氮气完全反应放出46kJ能量,
故答案为:放出;46;
(3)1mol氮气完全反应放出92kJ能量,则0.5mol氮气完全反应放出46kJ能量,该反应是可逆反应,反应物不能完全转化为生成物,所以放出的热量要小于46kJ,故答案为:该反应是可逆反应,反应物不能完全转化为生成物,所以放出的热量要小于46kJ;
(4)v(NH3)=$\frac{\frac{8mol}{2L}}{5min}$=0.8mol/(L.min),同一可逆反应中同一条件下不同物质的反应速率之比等于其计量数之比得v(N2)=$\frac{1}{2}$v(NH3)=$\frac{1}{2}$×0.8mol/(L.min)=0.4mol/(L.min),
故答案为:0.4;
(5)a.达到平衡状态时正反应速率和逆反应速率相等且不等于0,故正确;
b.达到平衡状态时,正反应速率和逆反应速率相等且不等于0,故错误;
c.达到平衡状态时,正逆反应速率相等,处于动态平衡状态,所以N2的转化率达到最大值,故正确;
d.N2和H2的浓度相等时该反应不一定达到平衡状态,与反应物初始浓度及转化率有关,故错误;
e.N2、H2和NH3的体积分数相等时,该反应不一定达到平衡状态,与反应物初始浓度及转化率有关,故错误;
f.达到平衡状态时,正逆反应速率相等,处于动态平衡状态,反应物的转化率达到最大值,所以反应达到最大限度,故正确;
故选bde.
点评 本题考查化学平衡计算、化学平衡状态判断等知识点,把握化学平衡状态特征、化学计算基本方法是解本题关键,注意:可逆反应达到平衡状态时正逆反应速率相等(同一物质)但不能是0,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ | |
| C. | 向氢氧化铜中滴加稀盐酸:Cu(OH)2+2H+═Cu2++2H2O | |
| D. | 锌粒与稀醋酸反应:Zn+2H+═Zn2++H2↑ |
2CoCl2•6H2O+10NH3+2NH4Cl+H2O2═2[Co(NH3)6]Cl3+14H2O
实验流程如图1:
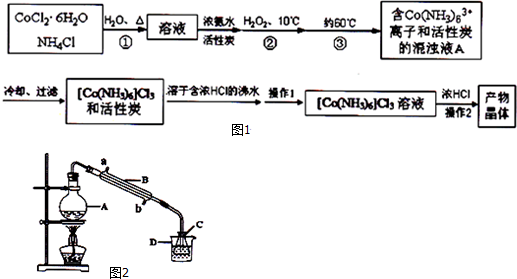
已知:[Co(NH3)6]Cl3 在水中电离为[Co(NH3)6]3+和Cl-,[Co(NH3)6]Cl3的溶解度如下表:
| 温度(℃) | 0 | 20 | 47 |
| 溶解度(g) | 4.26 | 6.96 | 12.74 |
(1)第①步需在煮沸NH4Cl溶液中加入研细的CoCl2•6H2O晶体,加热煮沸和研细的目的是加速固体溶解.
(2)H2O2的作用是做氧化剂,第③步中保持60℃的加热方法是水浴加热.
(3)过滤是滤纸先用蒸馏水湿润,然后用玻璃棒压实滤纸,排出滤纸与漏斗之间的气泡.
(4)实验操作1为趁热过滤,[Co(NH3)6]Cl3 溶液中加入浓HCl的目的是有利于[Co(NH3)6]Cl3析出,提高产率.
(5)现称取0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),在A中发生如下反应:
[Co(NH3)6]Cl3+3NaOH═Co(OH)3↓+6NH3↑+3NaCl(装置见图2),
C中装0.5000mol/L的盐酸25.00mL,D中装有冰水.加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,加入2~3滴甲基红指示剂,用0.5000mol/L的NaOH滴定.已知:
| 指示剂 | 颜色 | 变色的pH范围 | ||
| 甲基红 | 红 | 橙 | 黄 | 4.4~6.2 |
②当滴定到终点时,共需消耗NaOH溶液13.00mL(精确到0.01mL)
③若用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,则x值将偏大(填“偏大”、“偏小”或“不变”).
 反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )| A. | 上述反应是放热反应 | B. | 上述反应是吸热反应 | ||
| C. | a>b | D. | 增大压强,平衡向正反应方向移动 |