题目内容
5.下列关于能源的说法不正确的是( )| A. | 氢能源的优点是来源广泛、无污染、便于运输与贮存 | |
| B. | 自然界中利用太阳能最成功的是植物的光合作用 | |
| C. | 植物秸秆、动物粪便、枯枝败叶中蕴藏着丰富的生物质能 | |
| D. | 利用太阳能、风能和氢能替代化石能源能改善空气质量 |
分析 A.氢气易燃、易爆不利于储存;
B.植物通过光合作用可以将太阳能转化为植物有机能,进一步可以转化为生物质能;
C.生物质能就是太阳能以化学能形式贮存在生物质中的能量形式,即以生物质为载体的能量;
D.太阳能、风能和氢能的使用都不会产生环境污染.
解答 解:A.氢能源的优点是来源广泛、无污染,但是氢气易燃、易爆不利于储存和运输,故A错误;
B.自然界中利用太阳能最成功的是植物的光合作用,故B正确;
C.植物秸秆、动物粪便、枯枝败叶中蕴藏着丰富的生物质能,故C正确;
D.太阳能、风能和氢能的使用都不会产生环境污染,属于清洁能源,故D正确;
故选A.
点评 本题考查了能源的利用与开发,熟悉各类能源特点、明确常见能量转化形式是解题关键,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
15.咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为: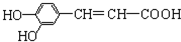 下列有关咖啡酸的说法中,不正确的是( )
下列有关咖啡酸的说法中,不正确的是( )
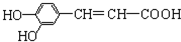 下列有关咖啡酸的说法中,不正确的是( )
下列有关咖啡酸的说法中,不正确的是( )| A. | 1 mol咖啡酸可与3 mol NaOH发生反应 | |
| B. | 咖啡酸可以发生还原、酯化、加聚、显色等反应 | |
| C. | 1 mol咖啡酸可与4 mol Br2发生反应 | |
| D. | 1 mol咖啡酸最多可与5 mol H2发生加成反应 |
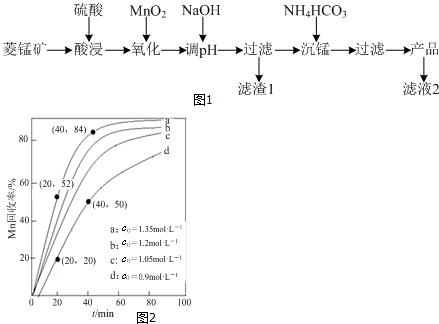
16.某地有软锰矿和闪锌矿两座矿山,它们的组成(质量分数)如表:
科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示.
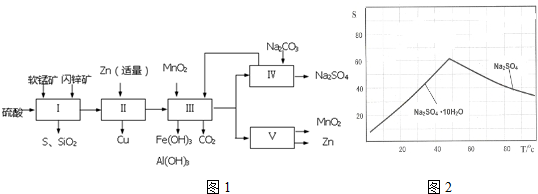
(1)流程Ⅰ所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等,则流程Ⅰ中被氧化的物质有FeS、CuS种.
(2)流程Ⅱ中反应的离子方程式为Zn+Fe3+=Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+.
(3)氢氧化物开始沉淀的pH如表:
流程Ⅲ中MnO2的作用是将Fe2+氧化成Fe3+,不直接生成Fe(OH)2沉淀的原因是使铁元素能全部沉淀.
(4)如图2是Na2SO4和Na2SO4•10H2O的溶解度(g/100g水)曲线,又知MnSO4和ZnSO4的溶解度随温度的升高而增大,则流程Ⅳ得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶、趁热过滤、乙醇洗涤、干燥,要“趁热”过滤的原因是防止形成Na2SO4•10H2O.
(5)流程Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为Mn2+-2e-+2H2O=MnO2+4H+.
(6)取1.95g锌加入到12.00mL 18.4mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000mL,取出15.00mL,以酚酞为指示剂,用0.25mol/L的NaOH溶液滴定余酸,耗用NaOH溶液的体积为21.70mL.
①反应后溶液中多余的硫酸是0.18 mol.
②通过计算确定浓硫酸被还原的产物是S.
| 软锰矿 | 闪锌矿 |
| MnO2约70%,SiO2约20%,Al2O3约4%,其余为水分 | ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分 |

(1)流程Ⅰ所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等,则流程Ⅰ中被氧化的物质有FeS、CuS种.
(2)流程Ⅱ中反应的离子方程式为Zn+Fe3+=Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+.
(3)氢氧化物开始沉淀的pH如表:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 7.6 |
(4)如图2是Na2SO4和Na2SO4•10H2O的溶解度(g/100g水)曲线,又知MnSO4和ZnSO4的溶解度随温度的升高而增大,则流程Ⅳ得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶、趁热过滤、乙醇洗涤、干燥,要“趁热”过滤的原因是防止形成Na2SO4•10H2O.
(5)流程Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为Mn2+-2e-+2H2O=MnO2+4H+.
(6)取1.95g锌加入到12.00mL 18.4mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000mL,取出15.00mL,以酚酞为指示剂,用0.25mol/L的NaOH溶液滴定余酸,耗用NaOH溶液的体积为21.70mL.
①反应后溶液中多余的硫酸是0.18 mol.
②通过计算确定浓硫酸被还原的产物是S.
20.向含有下列各组离子的溶液中滴加NaOH溶液,得到白色沉淀的是( )
| A. | Ba2+ HCO3- K+ Cl- | B. | CO32- OH- Na+ NO3- | ||
| C. | OH- Na+ SO42- CO32- | D. | Cu2+ Cl- Na+ NO3- |
10.酯化反应与水解反应均需要使用催化剂,下列有关说法正确的是( )
| A. | 酯化与水解反应均要用浓硫酸作催化剂 | |
| B. | 酯化与水解反应均可用Na0H作催化 | |
| C. | 酯类物质可用Na0H作催化剂,不宜用浓硫酸作催化剂 | |
| D. | 酯化反应使用浓硫酸作催化剂有利于反应向左进行 |
17.能正确表示下列反应的离子方程式的是( )
| A. | NH4Fe(SO4)2加入过量NaOH溶液中::NH4++Fe3++4OH-═NH3•H2O+Fe(OH)3↓ | |
| B. | 次氯酸钠溶液中通入过量的二氧化硫:ClO-+SO2+H2O═HSO3-+HClO | |
| C. | Ba(OH)2溶液和稀硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 澄清的石灰水中加入过量的NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
4.下列溶液中:①石灰水 ②H2S溶液 ③KMnO4溶液④酸化的Ba(NO3)2溶液 ⑤溴水 ⑥品红溶液,不能区别SO2和CO2气体的是( )
| A. | 只有① | B. | ①③ | C. | ①②③⑤ | D. | ②③④⑤ |