题目内容
常温下c(H+)最小的是( )
| A、pH=0的溶液. |
| B、0.03 mol?L-1 H2SO4. |
| C、0.05 mol?L-1 HClO |
| D、0.05 mol?L-1的NaHSO4. |
考点:物质的量浓度的相关计算
专题:
分析:A.根据pH=-lgc(H+)计算c(H+);
B.硫酸完全电离,溶液中c(H+)=2c(H2SO4);
C.HClO是弱电解质,不能完全电离,溶液中c(H+)<c(HClO);
D.NaHSO4完全电离,溶液中c(H+)=c(NaHSO4).
B.硫酸完全电离,溶液中c(H+)=2c(H2SO4);
C.HClO是弱电解质,不能完全电离,溶液中c(H+)<c(HClO);
D.NaHSO4完全电离,溶液中c(H+)=c(NaHSO4).
解答:
解:A.pH=-lgc(H+)=0,则c(H+)=1mol/L;
B.硫酸完全电离,溶液中c(H+)=2c(H2SO4)=0.06mol/L;
C.HClO是弱电解质,不能完全电离,溶液中c(H+)<c(HClO)=0.05mol/L;
D.NaHSO4完全电离,溶液中c(H+)=c(NaHSO4)=0.05mol/L,
故0.05mol?L-1HClO溶液中c(H+)最小,
故选C.
B.硫酸完全电离,溶液中c(H+)=2c(H2SO4)=0.06mol/L;
C.HClO是弱电解质,不能完全电离,溶液中c(H+)<c(HClO)=0.05mol/L;
D.NaHSO4完全电离,溶液中c(H+)=c(NaHSO4)=0.05mol/L,
故0.05mol?L-1HClO溶液中c(H+)最小,
故选C.
点评:本题考查物质的量浓度计算,比较基础,注意理解电解质浓度与电解质离子的浓度的关系,注意区分强弱电解质.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
下列标明电子转移的方向和数目的化学方程式中正确的是( )
A、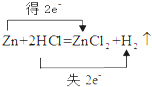 |
B、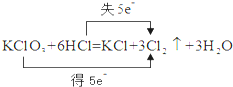 |
C、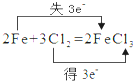 |
D、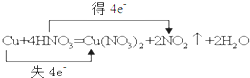 |
某元素基态原子的外围电子排布为3d54s2,则下列说法不正确的是( )
| A、该元素为Mn元素 |
| B、该元素原子核外有4个能层 |
| C、该元素原子最外层共有7个电子 |
| D、该元素属于d区元素 |
设阿伏加德罗常数为6.02×1023mol-1,关于1molH2O的叙述正确的是( )
| A、含有1molH2 |
| B、含有6.02×1023个水分子 |
| C、质量为18g/mol |
| D、在标准状况下的体积为22.4L |
能正确表示下列反应的离子方程式是( )
| A、Na2O2加入水制备O2:2O22-+2H2O=4OH-+O2↑ |
| B、用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| D、向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |