题目内容
8.某炼金厂的废水因连降暴雨而溢出,导致河水严重污染,炼金废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸.下列说法不正确的是( )| A. | CN-可以和稀硫酸反应生成HCN | B. | CN-可被Cl2氧化成(CN)2 | ||
| C. | 在水溶液中(CN)2不能将F-氧化 | D. | HCN的电子式为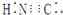 |
分析 A.硫酸的酸性大于HCN,可发生强酸制取弱酸的反应;
B.CN-的还原性介于I-与Br-之间,可被氯气氧化;
C.(CN)2的氧化性弱于单质氟的氧化性;
D.HCN的结构式为H-C≡N.
解答 解:A.HCN为弱酸,则根据较强酸制备较弱酸的原理可知,CN-可以和稀硫酸反应生成HCN,故A正确;
B.CN-还原性介于I-与Br-之间,所以能被氯气氧化生成(CN)2,故B正确;
C.(CN)2的氧化性弱于单质氟的氧化性,因此在水溶液中(CN)2不能将F-氧化,故C正确;
D.HCN的电子式应该是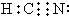 ,故D错误;
,故D错误;
故选D.
点评 本题考查物质的性质及应用,为高频考点,把握习题中的信息、卤素单质的氧化性比较为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的应用,题目难度不大.

练习册系列答案
相关题目
18.下列有机物不能通过加成反应制取的是( )
| A. | CH3CH2Cl | B. | CH2Cl-CH2Cl | C. | CH3-CH2OH | D. | CH3 Cl |
16.对于反应A(g)+3B(g)?2C(g)+2D(g),下列四个数据是在不同条件下测出的该反应的化学反应速率,其中最快的是( )
| A. | v(D)=0.4mol/(L•s) | B. | v(C)=30mol/(L•min) | C. | v(B)=0.4mol/(L•min) | D. | v(A)=0.15mol/(L•s) |
13.下列变化属于物理变化的是( )
| A. | 分馏 | B. | 干馏 | C. | 裂化 | D. | 裂解 |
20.设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 含4molHCl的浓盐酸与足量MnO2混合加热,产生NA个Cl2 | |
| B. | 氧气和臭氧组成的4.8g混合气体中含有0.3 NA个氧原子 | |
| C. | 标准状况下,2.24L SO3含有分子的数目为0.1NA | |
| D. | 1mol 硫酸氢钠溶液中含有阳离子数为NA |
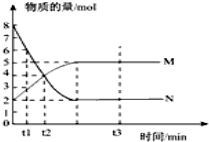 一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图示.
一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图示.
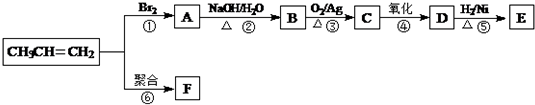
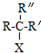 $\stackrel{NaOH/H_{2}O}{→}$
$\stackrel{NaOH/H_{2}O}{→}$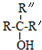 (X为卤素原子,R,R′,R″均为烃基或H原子)
(X为卤素原子,R,R′,R″均为烃基或H原子)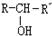 $\stackrel{O_{2}/Ag}{→}$
$\stackrel{O_{2}/Ag}{→}$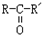 ,
,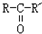 $\stackrel{H_{2}/Ni}{→}$
$\stackrel{H_{2}/Ni}{→}$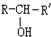
 ; D的结构简式是O=C(CH3)COOH.
; D的结构简式是O=C(CH3)COOH. .
.