题目内容
8.下列离子方程式正确的是( )| A. | 澄清石灰水中加盐酸:2H++Ca(OH)2═Ca2++2H2O | |
| B. | 向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-═CO32-+H2O | |
| C. | 氯气溶于水:Cl2+H2O?2H++ClO-+Cl- | |
| D. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
分析 A.澄清石灰水中的氢氧化钙应该拆开;
B.碳酸氢钠与氢氧化钠溶液反应生成碳酸钠和水;
C.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
D.氢离子、氢氧根离子的计量数错误.
解答 解:A.澄清石灰水中加盐酸,氢氧化钙应该拆开,正确的离子方程式为:H++OH-═H2O,故A错误;
B.向NaHCO3溶液中加入NaOH溶液,反应的离子方程式为:HCO3-+OH-═CO32-+H2O,故B正确;
C.氯气溶于水生成氯化氢和次氯酸,次氯酸不能拆开,正确的离子方程式为:Cl2+H2O?H++HClO+Cl-,故B错误;
D.向Ba(OH)2溶液中滴加稀硫酸,反应生成硫酸钡沉淀和水,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
4.下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是( )
| A. | Na和O2 | B. | NaOH和SO2 | C. | NaHCO3和NaOH | D. | Na2CO3和HCl |
16.下列物质的水溶液因水解呈酸性的是( )
| A. | SO2 | B. | AlCl3 | C. | NaHCO3 | D. | NaHSO4 |
20.下列分散系中,能产生“丁达尔效应”的是( )
| A. | Na2SO4溶液 | B. | NH4Cl溶液 | C. | 石灰乳 | D. | Fe(OH)3胶体 |
17.升髙温度能加快反应速率的主要原因是( )
| A. | 活化分子的能量明显增加 | B. | 改变了化学反应的能量变化 | ||
| C. | 降低了反应的活化能 | D. | 增加了活化分子的百分数 |
18.X、Y、Z、W四种气体都是污染大气的物质,其中Y跟W按一定体积比相遇时可消除气体的毒性;Y跟Z相遇时,可使气体的红棕色变浅;Y与Z分别是引起酸雨的主要物质,这四种气体依次是( )
| A. | H2S、NO、HCl、SO2 | B. | SO2、HCl、NO2、H2S | C. | H2S、NO2、Cl2、SO2 | D. | Cl2、SO2、NO2、H2S |
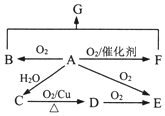 已知A石油裂解的主要产物,相对分子质量为28.B为气体,在标准状况下的密度为1.96g/L.D与F互为同分异构体,F是环状化合物.G的结构简式为:
已知A石油裂解的主要产物,相对分子质量为28.B为气体,在标准状况下的密度为1.96g/L.D与F互为同分异构体,F是环状化合物.G的结构简式为: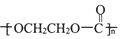 ,在一定条件下,它们有如图转化关系.
,在一定条件下,它们有如图转化关系.