题目内容
可逆反应:mA(s)+nB(g) qC(g),在一定温度的密闭容器中进行,B的体积分数(V(B)%)与压强的关系如图所示。下列叙述中正确的是( )
qC(g),在一定温度的密闭容器中进行,B的体积分数(V(B)%)与压强的关系如图所示。下列叙述中正确的是( )

A.m+n<q B.m+n>q C.n>q D.x点时,v(正)>v(逆)
练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
9.分子式为C8H10的芳香烃有( )种.
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
10.X、Y、Z、W是原子序数依次增大的4种短周期元素.X与Z位于同一主族,X原子的最外层电子数是次外层电子数的2倍,Y元素的单质既能与盐酸反应又能与NaOH溶液反应,X、Y、Z、W原子的最外层电子数之和为18.下列说法不正确的是( )
| A. | X单质在一定条件下能与Z的最高价氧化物发生置换反应 | |
| B. | 原子半径:Y>Z>W | |
| C. | 最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W | |
| D. | 室温下,0.1mol/LW的气态氢化物的水溶液的pH=1 |
6.下列有机化合物中,可以看作醇类的是( )
| A. | 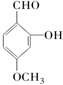 | B. |  | ||
| C. | 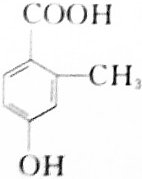 | D. | 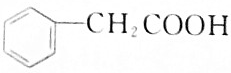 |
13.碳、氮及其化合物在工农业生产生活中有着重要作用.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,这是目前使用最广泛的人工固氮的方法.请回答下列问题:
450℃时,往一个2L的密闭容器中充入2.6molH2和1molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示
(1)5min内,消耗N2的平均反应速率为0.008mol.L-1.min-1
此条件下该反应的化学平衡常数值为0.1
(2)若改变某一条件,达新平衡时n(H2)=1.6mol,下列说法正确的是BD
A.平衡一定正向移动
B.可能是降低了容器的温度
C.可能是向容器中加入了一定量的H2气体
D.可能是缩小了容器的体积
(3)另一种人工固氮的新方法是在光照条件下,N2在催化剂表面与水蒸气发生反应生成NH3和O2. 已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-489kJ/mol
请根据以上信息,写出人工固氮新方法的热化学方程式2N2(g)+6H2O(g)=4NH3(g)+3O2(g)△H=1282.2KJ/mol
工业上也可在碱性溶液中通过电解的方法实现上述反应,阳极的电极反应式为4OH--4e-=O2↑+2H2O
(4)如图1表示500℃、60.0MPa条件下,合成氨原料气投料比与平衡时NH3体积分数的关系.根据图中a点数据计算N2的平衡体积分数:14.5%.
(5)通过NOx传感器可监测NOx的含量,其工作原理示意图如图2: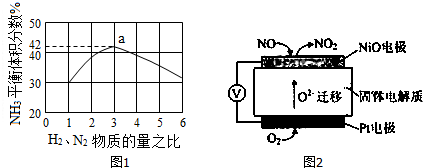
写出NiO电极的电极反应式:NO+O2--2e-=NO2
(6)①2NH3(g)+CO2(g)?NH2COONH4(s),此反应温度越低越容易自发进行,则该反应正向为放热反应(填“吸”或“放”).若将一定量NH2COONH4(s)置于恒温密闭容器中,其分解达到平衡状态,此时容器内压强为P1,混合气体的密度为ρ1.缩小容器的容积,再次达平衡时,容器内压强为P2,混合气体的密度为ρ2.则P1<P2(填“>”“=”或“<”),ρ1<ρ2(填“>”“=”或“<”).
②在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)?2C(g)+D(s)反应,按如表数据投料,反应达到平衡状态,测得体系压强升高.简述该反应的平衡常数与温度的变化关系:升高温度平衡常数减小
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,这是目前使用最广泛的人工固氮的方法.请回答下列问题:
450℃时,往一个2L的密闭容器中充入2.6molH2和1molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.2 | 0.2 | 0.2 |
此条件下该反应的化学平衡常数值为0.1
(2)若改变某一条件,达新平衡时n(H2)=1.6mol,下列说法正确的是BD
A.平衡一定正向移动
B.可能是降低了容器的温度
C.可能是向容器中加入了一定量的H2气体
D.可能是缩小了容器的体积
(3)另一种人工固氮的新方法是在光照条件下,N2在催化剂表面与水蒸气发生反应生成NH3和O2. 已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-489kJ/mol
请根据以上信息,写出人工固氮新方法的热化学方程式2N2(g)+6H2O(g)=4NH3(g)+3O2(g)△H=1282.2KJ/mol
工业上也可在碱性溶液中通过电解的方法实现上述反应,阳极的电极反应式为4OH--4e-=O2↑+2H2O
(4)如图1表示500℃、60.0MPa条件下,合成氨原料气投料比与平衡时NH3体积分数的关系.根据图中a点数据计算N2的平衡体积分数:14.5%.
(5)通过NOx传感器可监测NOx的含量,其工作原理示意图如图2:

写出NiO电极的电极反应式:NO+O2--2e-=NO2
(6)①2NH3(g)+CO2(g)?NH2COONH4(s),此反应温度越低越容易自发进行,则该反应正向为放热反应(填“吸”或“放”).若将一定量NH2COONH4(s)置于恒温密闭容器中,其分解达到平衡状态,此时容器内压强为P1,混合气体的密度为ρ1.缩小容器的容积,再次达平衡时,容器内压强为P2,混合气体的密度为ρ2.则P1<P2(填“>”“=”或“<”),ρ1<ρ2(填“>”“=”或“<”).
②在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)?2C(g)+D(s)反应,按如表数据投料,反应达到平衡状态,测得体系压强升高.简述该反应的平衡常数与温度的变化关系:升高温度平衡常数减小
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |


 A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )
A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )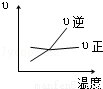 B.
B.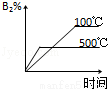 C.
C.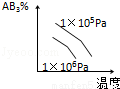 D.
D.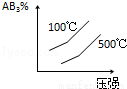
 O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)
O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)