题目内容
将乙酸(其中的氧都18O标记)在浓硫酸存在条件下与足量的乙醇充分反应.下叙述不正确的是( )
| A、生成是水分子中含有18O |
| B、生成的乙酸乙酯相对分子质量为88 |
| C、生成的乙酸乙酯的相对分子质量为90 |
| D、此反应是有限度的 |
考点:乙酸乙酯的制取
专题:有机反应
分析:依据有机酯化反应的实质是酸脱羟基醇脱氢的反应原理、在浓硫酸存在下并加热酯化反应属于可逆反应分析判断.
解答:
解:将1mol乙酸在浓硫酸存在条件下与足量乙醇充分反应,酸脱羟基醇脱氢,化学方程式为:CH3C18O18OH+HOCH2CH3
CH3C18OOCH2CH3+H218O;
A.生成的水分子中含有18O,故A正确;
B.生成的乙酸乙酯中含有18O,故生成的乙酸乙酯的相对分子质量为90,故B错误;
C.生成的乙酸乙酯中含有18O,故生成的乙酸乙酯的相对分子质量为90,故C正确;
D.乙酸和乙醇反应生成乙酸乙酯是可逆反应,所以不能进行彻底,故D正确;
故选B.
| 浓硫酸 |
| △ |
A.生成的水分子中含有18O,故A正确;
B.生成的乙酸乙酯中含有18O,故生成的乙酸乙酯的相对分子质量为90,故B错误;
C.生成的乙酸乙酯中含有18O,故生成的乙酸乙酯的相对分子质量为90,故C正确;
D.乙酸和乙醇反应生成乙酸乙酯是可逆反应,所以不能进行彻底,故D正确;
故选B.
点评:本题考查了酯化反应的反应实质,关键是反应历程和可逆反应的应用,题目较简单.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
有下列三个反应:下列说法正确的是( )
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br-
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br-
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.
| A、反应①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B、根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3 |
| C、在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化 |
| D、可以推理得到Cl2+FeBr2═FeCl2+Br2 |
下列离子方程式书写正确的是( )
| A、AlCl3溶液滴加过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++H2O |
| B、硫酸和氢氧化钡溶液反应:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
| C、向氢氧化铁胶体中滴加足量HI溶液:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| D、向氯化钙溶液中通入CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
下列离子方程式或化学反应方程式与所述事实相符且正确的是( )
| A、将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+QkJ/mol |
| B、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO |
| C、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D、向含有0.4molFeBr2的溶液中通入0.3molCl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
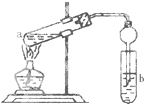 如图,在试管a中先加入3mL 95%的乙醇,边摇动边缓缓加入2mL浓H2SO4并充分摇匀,冷却后再加入2mL冰醋酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入3mL 95%的乙醇,边摇动边缓缓加入2mL浓H2SO4并充分摇匀,冷却后再加入2mL冰醋酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.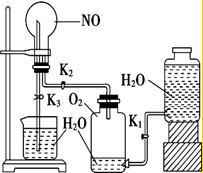 某学生设计了一套验证物质化学性质的实验装置(如图),请观察该装置图,完成下列问题:
某学生设计了一套验证物质化学性质的实验装置(如图),请观察该装置图,完成下列问题: