题目内容
17.某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M离子,经测定Fe3+、SO42-、Al3+和M离子的物质的量之比为1:4:1:2,则M离子可能是下列中的( )| A. | Na+ | B. | OH- | C. | S2- | D. | Ag+ |
分析 Ag+与SO42-生成微溶的硫酸银,M不能为Ag+离子,S2-与Fe3+发生氧化反应,与Al3+发生水解反应反应生成氢氧化铝与硫氢化,则M不能为S2-,而OH-与Fe3+、Al3+生成氢氧化铁、氢氧化铝沉淀,故M也不能是OH,再结合电荷守恒进行验证.
解答 解:Ag+与SO42-生成微溶的硫酸银,M不能为Ag+离子,S2-与Fe3+发生氧化反应,与Al3+发生水解反应反应生成氢氧化铝与硫氢化,则M不能为S2-,而OH-与Fe3+、Al3+生成氢氧化铁、氢氧化铝沉淀,故M也不能是OH,M可能为Na+,3n(Fe3+)+n(Na+)+3n(Al3+)=8,2n(SO42-)=8,则3n(Fe3+)+n(Na+)+3n(Al3+)=2n(SO42-),符合电荷守恒,
故选:A.
点评 本题考查离子构成、物质的量有关计算,只利用离子共存即可排除确定,注意混合溶液中常利用电荷守恒计算离子物质的量.

练习册系列答案
相关题目
8.NA表示阿伏加德罗常数,则下列说法正确的是( )
| A. | 2.4g Mg变成Mg2+时失去的电子数为0.1 NA | |
| B. | 标准状况下,11.2 L水所含的原子数为1.5 NA | |
| C. | 在常温常压下,32g氧气所含原子数目为2NA | |
| D. | 0.1mol/LK2SO4溶液含有 K+0.2 NA |
5.如下表所示将a溶液逐滴加入装有b溶液的试管中,下列现象对应的离子方程式错误的是( )
| 选项 | a | b | 试管中现象 | 离子方程式 |
| A | 硫酸 | KI淀粉 | 在空气中放置一段时间后溶液呈蓝色 | 4H++4I-+O2═2I2+2H2O |
| B | 稀盐酸 | Na2CO3 | 开始时无气泡,后来有气泡 | CO32-+H+═HCO3-; HCO3-+H+═H2O+CO2↑ |
| C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++SiO32-═H2SiO3(胶体) |
| D | 硫酸 | 滴有酚酞的Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
12.元素的最高价氧化物溶于水,形成的含氧酸的酸性最强的是( )
| A. | 原子最外层电子数是次外层的2倍的元素 | |
| B. | 原子M层电子数等于另两层电子数之差的元素 | |
| C. | 第三周期ⅦA族的元素 | |
| D. | 其单质有多种同素异形体,其中一种着火点很低、能自燃的元素 |
6.下列离子在可使酚酞变红的、无色透明的溶液中,能大量共存的是( )
| A. | K+、Ba2+、Cl-、NO3- | B. | Na+、Cu2+、SO42-、OH- | ||
| C. | Na+、Cl-、Ca2+、MnO4- | D. | Na+、HCO3-、SO42-、Cl- |
20.下列离子方程式书写正确的是( )
| A. | 向硫酸酸化的FeSO4溶液中加入过量的H2O2溶液:2Fe2++H2O2+2H+═2Fe3++2H2O | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 碳酸镁与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
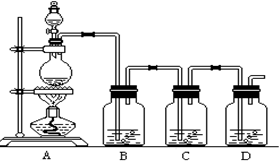
 合成氨的流程示意图如图:回答下列问题:
合成氨的流程示意图如图:回答下列问题: