题目内容
18.工业制硫酸中的一步重要反应是SO2(在400-500℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法错误的是( )| A. | 在上述条件下,SO2可能100%的转化为SO3 | |
| B. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| C. | 达到平衡时,SO2与SO3的浓度保持不变 | |
| D. | 为了提高SO2的转化率,可以适当提高O2的浓度 |
分析 根据该反应是前后气体体积减小的放热反应,利用外界条件对化学平衡的影响因素分析,
A.在上述条件下,可逆反应,SO2少于100%的转化为SO3;
B.使用催化剂是为了加快反应速率,提高生产效率;
C.达到平衡时,SO2与SO3的浓度保持不变;
D.为了提高SO2的转化率,可以适当提高O2的浓度,使平衡正向移动.
解答 解:A、因该反应是可逆反应,存在反应限度,反应物不可能100%的转化,故A错误;
B、使用催化剂加快了反应速率,缩短反应时间,提高反应效率,平衡不移动,故B正确;
C、达到平衡时,各组分的浓度保持不变,故C正确;
D、因增大反应物O2的浓度,平衡向正反应方向移动,提高了SO2的转化率,故D正确.
故选:A.
点评 本题考查了影响化学平衡移动的因素,难度不大,注意催化剂只影响化学反应速率不影响化学平衡移动.

练习册系列答案
相关题目
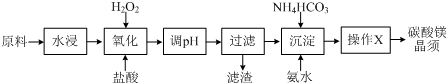
9.碳酸镁晶须是一种新型吸波隐形材料中的增强剂.某工厂以MgCl2(含少量杂质FeCl2、FeCl3)为原料制备碳酸镁晶须(MgCO3•H2O)的工艺流程如下:
已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
注:Fe(OH)2沉淀呈絮状,不易从溶液中除去.
(1)写出“氧化”过程中发生的离子反应方程式并用单线桥标出电子转移的方向和数目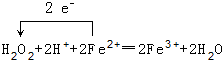 .
.
(2)pH调节的范围3.7~9.9之间,滤渣的主要成分Fe(OH)3(填化学式).
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法取最后一次洗涤液,加入硝酸酸化,再加入硝酸银溶液,没有白色沉淀生成,说明洗涤干净.
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00mL,测得Cl-的浓度为0.455mol•L-1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl-的浓度为0.460mol•L-1(溶液体积变化忽略不计).
②另取水浸后溶液100.00mL,向其中加入过量的1mol•L-1NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96g.
试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度(写出计算过程).

已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mg(OH)2 | 9.9 | 11.1 |
(1)写出“氧化”过程中发生的离子反应方程式并用单线桥标出电子转移的方向和数目
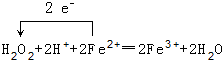 .
.(2)pH调节的范围3.7~9.9之间,滤渣的主要成分Fe(OH)3(填化学式).
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法取最后一次洗涤液,加入硝酸酸化,再加入硝酸银溶液,没有白色沉淀生成,说明洗涤干净.
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00mL,测得Cl-的浓度为0.455mol•L-1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl-的浓度为0.460mol•L-1(溶液体积变化忽略不计).
②另取水浸后溶液100.00mL,向其中加入过量的1mol•L-1NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96g.
试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度(写出计算过程).
13.煤化工中常需研究不同温度下的平衡常数、投料比及产率等问题,提高一氧化碳制取氢气的产率是其重要研究之一.
(1)已知:
C(石墨)+$\frac{1}{2}$O2(g)=CO(g)△H1=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-242kJ/mol
C(石墨)+O2(g)=CO2(g)△H3=-394kJ/mol
请写出一氧化碳那与水作用转化为氢气和二氧化碳反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol;
(2)能判断该反应达到化学平衡状态的依据是( )(填序号);
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)已知一氧化碳与水作用转化为氢气和二氧化碳的化学平衡常数随温度的变化如下表:
在800℃时,2L的密闭容器中加入4molCO(g)和6molH2O(g),10min后达到平衡时CO2的平衡浓度为1.2mol/L,用H2浓度变化来表示的平均反应速率为0.12mol/(L•min),CO的转化率是60%;
(4)为使该反应的速率增大且平衡向正反应方向移动,可采取的措施是A.
A.增大CO浓度 B.升高温度
C.将生成物分离出去 D.使用高效催化剂.
(1)已知:
C(石墨)+$\frac{1}{2}$O2(g)=CO(g)△H1=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-242kJ/mol
C(石墨)+O2(g)=CO2(g)△H3=-394kJ/mol
请写出一氧化碳那与水作用转化为氢气和二氧化碳反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol;
(2)能判断该反应达到化学平衡状态的依据是( )(填序号);
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)已知一氧化碳与水作用转化为氢气和二氧化碳的化学平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(4)为使该反应的速率增大且平衡向正反应方向移动,可采取的措施是A.
A.增大CO浓度 B.升高温度
C.将生成物分离出去 D.使用高效催化剂.
10.下列离子方程式不正确的是( )
| A. | 向偏铝酸钠溶液中加入过量盐酸:AlO2-+4H+=Al3++2H2O | |
| B. | MnO2与浓盐酸混合加热:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 等浓度等体积的Ba(OH)2溶液和NaHSO4溶液混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | 用NaOH溶液吸收少量H2S气体:OH-+H2S=HS-+H2O |
7.下列说法不正确的是( )
| A. | 锡中加入一定量的铅制成焊锡,目的使被焊接的部分更牢固,更不易被氧化 | |
| B. | 聚乙烯制成塑料薄膜,用于食品、药品包装的材料 | |
| C. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
8.某元素X的原子序数为52,下列叙述正确的是( )
| A. | X的主要化合价是-2、+4、+6 | |
| B. | 可以形成稳定的气态氢化物 | |
| C. | X的最高价氧化物对应水化物的酸性比HBrO4的酸性强 | |
| D. | X原子的还原性比碘原子强 |
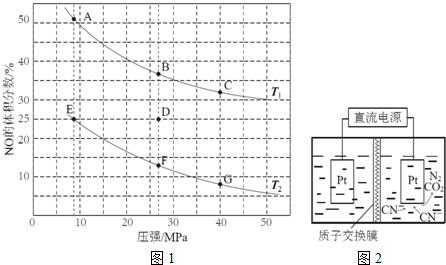
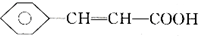 ),继而合成H的路线如下:
),继而合成H的路线如下: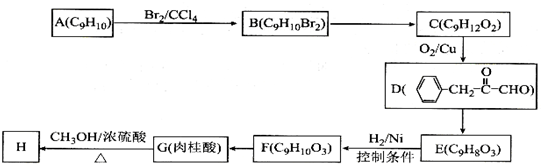
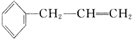 ,D中含有官能团的名称为羰基、醛基;
,D中含有官能团的名称为羰基、醛基; +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$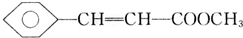 +H2O;
+H2O;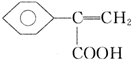 、
、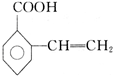 、
、 、
、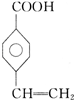 .
.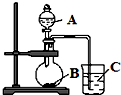 某研究性学习小组设计了一组实验,验证元素周期律.
某研究性学习小组设计了一组实验,验证元素周期律.